快速检测疯牛病
“在发病前快速检测出受感染的牲畜,对消除恐慌意义重大。”Stanley B.Prusiner
2003年12月,疯牛病初袭美国,联邦官员宣布来自华盛顿州的霍斯坦种乳牛感染了牛海绵状脑病(疯牛病)。这一消息使得科学家、政府官员、畜牧业和媒体在刚刚过去的那个新年中争相抢夺最新情报。但是,对于我们这些研究疯牛病及其他脑损伤引发的致命疾病的人来说,发现得病的动物是件很平常的事情。这种病的根源是Prion(朊病毒),很久以前人们就已经认识到,朊病毒的奇异特性将会给疯牛病的控制和食品供应的安全保障带来困难。
虽然朊病毒可以潜伏数年甚至数十年而不出现症状,给研究工作带来了困难,但研究者还是找到了能行之有效地防止该疾病流行的办法。其关键是要有高度敏感的甚至可以检测到无症状个体中的朊病毒的检测方法。这些方法中有一些已开始应用于临床,另一些尚在研发中。目前疯牛病只能在动物自然死亡或者被宰杀之后才能进行诊断。研究者也在治疗人类致命性疾病:朊病毒病——克-雅病(CJD)方面取得了一些进展。
疯牛病的病因
在美国,尽管疯牛病才开始引起公众的关注,但对疯牛病及其相关疾病的科学研究却早已升温。1980年代早期,我曾经提出羊瘙痒症、克雅病的病原体是由一种称为朊病毒的蛋白质构成。朊病毒理论很长时间以来遭到人们的怀疑,因为它与经典理沦(具有复制能力的病原体必须包含DNA或RNA)相悖。我的理论遭到怀疑是很正常而且很重要的,因为大部分引人注目的新颖想法最终都被证明是错误的。然而,阮病毒概念成功了。
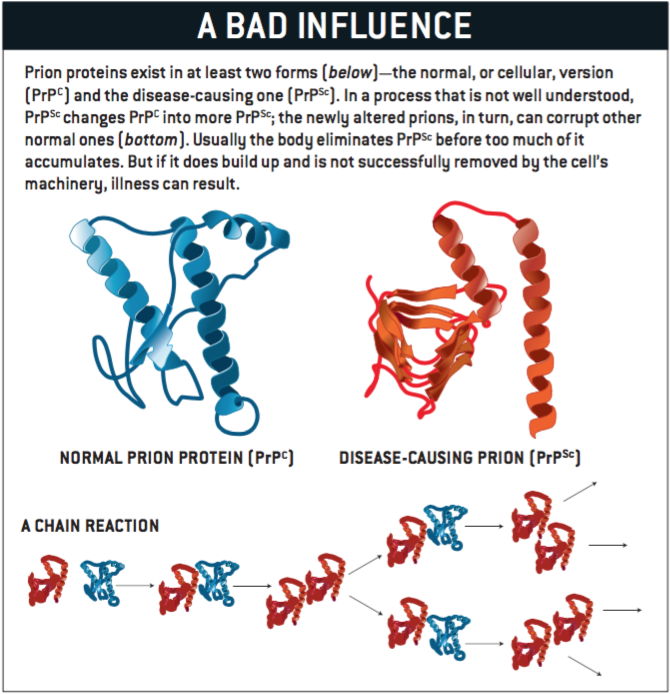
在我提出该理论后,研究人员取得的大量研究进展解释了这一引人注目的蛋白。我们知道阮病毒除了引起羊瘙痒症、克-雅病外,还会引起其他海绵状脑病,包括牛海绵状脑病以及鹿和麋鹿的慢性消耗性疾病。但最令人震惊的是:阮蛋白并不总是坏的。事实上,迄今为止所有的实验动物都有编码朊蛋白的基冈。朊蛋白的正常构象PrPC主要存在于神经细胞,可能有助于维持神经元的功能。但它可以转变成异常构象的PrPSc而引起疾病。
与正常构象不同的是,PrPSc易于形成难溶解的凝块,它对热、放射线、化学药品的抵抗力均强于其他病原体。细菌、病毒及霉菌在沸水中几分钟就可以被灭活,PrPSc却依然存活。PrPSc还可以诱导PrPC重新折叠而转化为PrPSc,产生更多异常构象的朊蛋白。虽然宿主细胞可以分解清除错误折叠的蛋白质,但是一旦清除PrPSc的速度慢于其产生的速度,就会造成PrPSc聚集,导致细胞破裂,表现出这类疾病的病理学改变一一脑部大量蛋白质沉积,镜下可见大量的空泡,呈现海绵状外观。同时也会表现出该病的症状。
朊病毒病以各种不同的方式折磨着人类和动物。大多数时候疾病是散发的,呈自发发病,没有明显的原因。散发性克-雅病是人类最常见的朊病毒病,发病率大约为1/1000,000,患者主要为老年人。编码朊蛋白的基因突变也可能导致朊病毒病;已知有很多家庭死于克-雅病、致死性家族性失眠症(fatalinsomnia)和格-施-沙综合征(Gerstmann-Straussler-Scheinker disease)。迄今为止,研究人员已经发现了朊蛋白基因30种突变可以导致遗传性疾病,它们都很罕见,发病率大约为1/10,000,000。朊病毒病还可由感染引起,比如通过食入含有朊病毒的牛肉,也会导致朊病毒病。
疯牛病流行史的回溯
自从1980年代中期疯牛病的爆发大肆破坏英国牛肉产业,世界开始意识到牛的阮病毒病的危险性。由朊病毒带来的全新的科学概念使研究人员和整个社会不得不从一种全新的角度去思考并且应付困难的流行问题。调查人员最终发现朊病毒是通过“肉骨餐”(meat-and-bone meal)在牛群中传播的,这是一种由一部分用于工业的羊、牛、猪和鸡通过加工、提炼而制成的补充食品。高温可以消灭常规的病原体,但PrPSc却能存活下来并继续感染牛群。
当感染的牛被制成饲料提供给其他牛的时候,疯牛病开始在全英国的牛群中出现,其确诊数在1992年高达37280例。英国的权威人士从1989年就开始制定一些饲养禁令,但直到1996年关于同类相食的严格的饲养禁令才控制住英国的疯牛病;去年英国只有612例病例。至今,英国确诊的病牛数为18万头,而流行病学模式显示的结果表明还有190万头乳牛已被感染但未被检出。
对于一些人来说,法令颁布得太晚了。与英国政府早先的保证相悖的是,疯牛病已被证实可以传给人类。1996年3月,爱丁堡的英国国家CJD监督部门的工作人员Robert Will、James Ironside和Jeanne Bell报告了11名英国青少年死于一种变异的克-雅病(vCJD)。在这些病人脑内沉积的PrPSc与典型的CJD患者脑内的存在明显的差异。
包括我在内的很多科学家最初都对疯牛病和vCJD之间可能存在的联系持怀疑态度。但基于大量研究,我最终改变了自己的看法。其中的一项研究就是我在美国加州大学旧金山分校的同事Michael Scott和Stephen De Armond完成的。他们改变了小鼠的基因,使它们对于朊蛋白的反应与牛相似(将牛的PrPSc基因插入小鼠的基因组),然后收集数据。这些小鼠在注入由患疯牛病的牛或患vCJD的人体内提取的朊病毒之后,在将近九个月的时候发病,而且来自人或者牛的朊病毒在小鼠体内导致的症状是相似的。截止至2004年2月,在英国已经有146人被诊断患有vCJD,在其他地区也有10名患者。没有人清楚还有多少人体内有导致vCJD的朊病毒处于潜伏期而没有发病。虽然流行病学模式显示,只有为数不多的人会发展vCJD患者,但是这些模式基于的假设可能本身就是错误的。举例来说,其中一个假设就是vCJD只感染那些有特异基因结构的个体。但由于朊病毒的潜伏期很长,所以我们还需要更长的时间来确定最终的vCJD病例数以及他们是否都有同样的基因类型。
在vCJD患者中,PrPSc不仅仅在脑中增加,在淋巴系统(如扁桃腺、阑尾)中也有所增加,说明PrPSc在某些地方可以进入血液。动物实验显示,朊病毒可以通过输血而由已感染的动物传给健康的动物。因此,很多国家已经颁布了更为严格的献血规定。在英国,1996年(也就是严格的饲养禁令实行的那一年)后出生的人,只能接受来自国外的血液(因为在这之前出生的人都有可能暴露于病毒之下)。在美国,1980至1996年之间在英国生活了3个月及以上的人不能献血。
虽然这样的规定会导致周期性的血源短缺,但这种方法被证明是合理的。去年12月,英国宣布在接受了vCJD患者的血液的15名受血者中,有一人已死于vCJD。但是,他的年龄使这一点不成立:他已经69岁了,比典型的vCJD患者的年龄(29岁)大了很多。因此,vCJD极有可能不只局限于食入朊病毒感染的牛肉的人群。
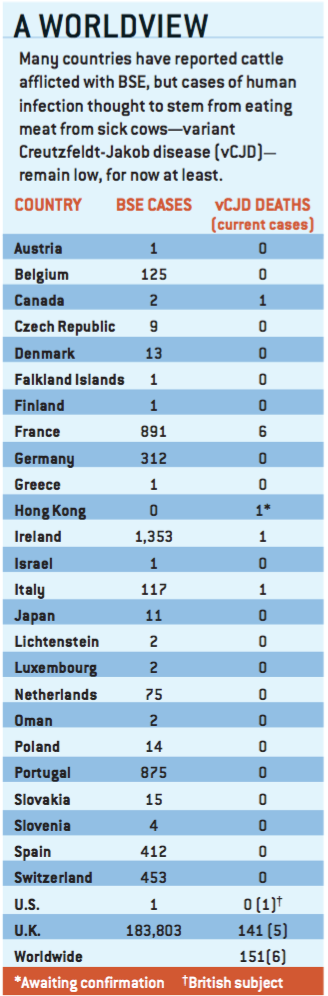
自英国发现了疯牛病,已经有20多个国家发现了病例。加拿大和美国是最后两个加入其中的。2003年5月20日,加拿大官员报告说一头八岁半的奶牛感染了疯牛病,而这头奶牛曾经在阿尔伯达省(Alberta)和萨斯喀彻温省(Saskatchewan)居留过。(此前加拿大唯一一例疯牛病是10年前由英国进口的。)虽然这头牛在2003年1月就被宰杀了,但是这种缓慢的处理意味着官员们直到4月才检验了这头牛。而在那个时候,它的肉早已被做成宠物食品出口到美国了。
7个月之后,在12月23日,美国农业部宣布该国在华盛顿省发现了第一例疯牛病。那是一头六岁半的奶牛,它在四岁的时候来到美国。这一发现说明美国官员不能再固守美国不存在疯牛病的错误观点了。像加拿大一样,美国农业经营者希望疯牛病可以消失。财政危机主要是源于牛肉出口的建设:58个国家关闭了边境,而30亿的出口市场就这么凭空蒸发了。
计划诊断学
对于本国和其他国家来说,保证安全的最直接方法看来很简单:只要检验被屠宰作为食物的动物,并禁止被感染的动物进入食品市场,防止它们将致病的朊病毒传播给人类即可,但实际工作却并不简单。美国农业部采用的是免疫组织化学的方法,这种陈旧的方法操作起来既繁琐又费时(需要几天才能完成),因此不适合在国际上应用。
因此,许多人都在寻求新的方法。1980年代中期研究人员研制出可以更有效地检测脑内朊病毒的新型抗体。与标准检测方法中的抗体一样,这些抗体也能识别任何的朊病毒(包括正常构象的和其他构象的朊病毒)。因此,为了检测到PrPSc,我们首先需要用蛋白酶降解脑样品中的所有PrPC。PrPSc可以抵抗蛋白酶的作用,因此它们大部分可以保持完好。接着在样品中加入抗体就可以显示存在PrPSc的量了。许多公司,包括瑞士的Prionic和法国的Bio-Rad,都用类似的方法生产出了他们自己的抗体和试剂盒。由于可以在几个小时内获得结果,所以在欧洲和日本,这些试剂盒应用于正在进行中的大规模筛查。(日本在2001年发现了首例疯牛病,截止到今年4月,一共发现了11例。)
但是这些快速的检测方法有一定的局限性。大多数时候,它们必须在动物脑内有相对较高水平的PrPSc积聚时才能检测出来。但疯牛病病程发展通常需要3到5年的时间,大多数牛被屠宰时还不到2岁,因此即使它们已经感染,检查结果也通常不呈阳性。因此,这些检测方法用于老牛的检测更可靠,不管它们看起来是健康或是虚弱。这时,最有可能选来进行检测的就是那些衰弱到不能自己站立的牛。
在今年1月的新规章出台之前,美国每年都有大约20万头虚弱的牛被屠宰供人们消费,其中只有一小部分是经过检测的。但明年美国农业部至少将检测20万头牛。(现在还不能确定牛奶会不会受到影响,我的实验室正在检测取自感染了海绵状脑病的牛的牛奶。)
由于现有检测方法的局限性,发展一种能从大量取自无症状小牛的牛肉中检测出朊病毒的方法仍然是我们对抗朊病毒病最重要的武器之一。
科学家主要以几种策略为基础进行了研究。一种是尝试提高样品中PrPSc的含量,以减少朊病毒逃过检测的可能。如果这种扩增系统能够创建成功,那就可以发展一种通过血液检查而不用杀死动物的方法(循环血液中的PrPSc含量不足以用现有的检测方法检测出来)。瑞士雪兰诺制药公司(Serono Pharmaceuticals)的Claudio Soto及其同事正在尝试将这个想法变成现实。他们将取自正常仓鼠和感染了海绵状脑病的仓鼠的脑组织样品混合在一起,然后用声脉冲将混合物中的PrPSc凝块打散,这样PrPSc就可以诱导正常构象的朊蛋白转换成致病的异常构象了。实验结果表明,能够抵抗蛋白酶的朊蛋白增加了10倍。美国达特茅斯医学院(Dart—mouth Medical School)的Surachai Supattapone也得到了类似的结果。
另一个策略关注的是朊蛋白复杂的构象而非数量,以我与美国加州大学旧金山分校的同事Jiri Safar进行的检测为例来说明。我们的方法是基于一种抗体,它可以与PrPC及PrPSc的其中之一结合。在一种构象下,朊蛋白上与这种抗体特异性结合的位点很容易被接近,但是改变构象后,这一结合位点就被包裹了起来(就像是床单的一角在折叠后就被藏起来了一样),因此也就无法与抗体相结合了。这种特异性说明待测样品不再需要经过蛋白酶的降解。去掉这一步是非常重要的,因为有一种构象的PrPSc对蛋白酶敏感,这就意味着在用蛋白酶除去PrPC的同时可能也除去了大部分或全部的蛋白酶敏感的PrPSc——所以这些检测方法也就将PrPSc的水平低估了90%。
我们研制出的检测方法,构象依赖性免疫测定方法(conformation—dependent immunoasay,CDI),于2003年被正式批准应用于欧洲。这种方法对于检测血液中的PrPSc可能具有足够的灵敏度。它已被批准应用于小牛的筛选。2003年秋天,日本报导了两例病牛分别为21和23个月大,它们都没有表现出明显的神经功能障碍。在23个月大的病牛中,两种商用方法都未能得出确切结果,而CDI则表明在脑干隐藏着致病的朊病毒。
在欧洲是不会发现这样的病例的,因为在那里只有超过30个月(在德国是24个月)的牛要被屠宰供人类消费时才必须进行检测。日本政府原本也打算采用欧盟的做法,但是消费者权益保护者促使政府改变了政策,对每一头要宰杀的动物都进行检测。由日本的例子我们可以看到,看似健康的动物也可能携带致病的朊病毒,因此我相信唯有对每一头要被屠宰的动物都进行检测才是最合理的政策。尽管到目前为止,所有的方法都还不够灵敏。但是,快速、灵敏的检测方法的出现意味着常规普查将成为可能。(我这么说看起来有给自己做广告的嫌疑,因为我在生产CDI的公司中有股份。但我确实还没有看到其他更好的方法可以使我们的食品安全得到更大的保障。)
一些新的洞见
在进行CDI的过程中,我们发现了朊病毒病的发展过程中一个惊人的事件。正如我刚才提到的那样,我们发现朊病毒其实是对蛋白酶的消化有着不同抵抗力的一系列蛋白质。同时,我们也发现对于蛋白酶敏感的PrPSc比蛋白酶抵抗型的PrPSc出现得早很多。至于蛋白酶敏感的PrPSc是不是生成蛋白酶抵抗的PrPSc过程的中间产物,暂时还没有定论。但无论如何,可以鉴别蛋白酶敏感型PrPSc的检测能在症状出现之前就发现感染,因此食品供应就会得到最大限度的安全保障,同时,感染的病人也可以更及时地得到救助。幸运的是,通过应用CDI,我的同事们和我可以检测到啮齿类和人类血液中低水平的蛋白酶敏感型PrPSc。
在血液中搜寻朊病毒的过程中,我们又发现了另一件惊人之事。美国科罗拉多大学医学部的Patrick Bosque和我发现小鼠后肢肌肉中的朊病毒水平是血液中的10万倍;其他肌群中也含有朊病毒,水平却低得多。但是,德国柏林的罗伯特·科赫研究所的Michael Beekes及其同事发现事实上食入朊病毒的仓鼠体内所有肌肉都含有PrPSc,且处于高水平,而不仅仅是在后肢。(我们不知道得到不同结果的原因,或者为什么后肢的肌肉会含有更多的朊病毒。)除了啮齿类动物之外,人类患者中也有同样的发现。加州大学旧金山分校的科学家Safar和De Armond发现一些CJD患者的肌肉内存在PrPSc,而瑞士苏黎世大学的Adriano Aguzzi等人发现在他们检查的CJD患者中,有25%的患者肌肉中存在PrPSc。

当然,最理想的朊病毒检测手段是非侵害性方法,例如尿检。但遗憾的是,到目前为止,唯一有希望的方法是在尿液中检测蛋白酶抵抗型PrP,随后的研究还无法证明其是否有效。
新疗法探讨
尽管新的诊断程序将提高食物和血源的安全性,但它无疑也会使被确诊患有这种致命疾病的人承受巨大的痛苦。因此,许多研究人员着眼于如何阻断朊病毒的形成或提高宿主细胞清除朊病毒的能力。迄今为止,研究人员已经发现20种可以抑制朊病毒形成或加强体外培养细胞清除朊病毒能力的化合物。相关研究表明,在给小鼠或仓鼠接种朊病毒时让它们服用上述的一些化合物,可以延长它们的生存时间,但在初次感染后给它们服用却不能改变他们的病程。此外,这些化合物中的一些在高剂量时才能发挥作用,这就意味着它们在动物体内会产生毒性作用。
与大剂量时的潜在毒性相比,更亟待解决的问题是寻找能透过血脑屏障、通过血流进入脑组织的药物。我和德国杜塞尔多夫大学的Carsten Korth、日本九州大学的堂浦克美以及美国国立过敏和传染病所的Byron Caughey分别找到了可以在脑内起作用的药物。例如,氯丙嗪(一种用于治疗精神分裂症的药物),可以在体外培养的细胞中抑制朊病毒形成。另一种化合物奎那克林,是一种与氯丙嗪结构相似的抗疟药,作用却约是氯丙嗪的10倍。
在动物实验中,奎那克林已经显示出一定的作用。我和同事在给小鼠脑部注射朊病毒60天后开始给它们服用奎那克林,发现潜伏期(从感染到出现疾病症状的时间)较对照组(未服用奎那克林)延长了约20%。如果病人能够耐受治疗所需要的高剂奎那克林或其他效力更强的相关药物被研制出来的话,那么这一“延长”对他们来说就是非常有意义的。我在加州大学旧金山分校的同事Barnaby May和E. Cohen致力于药效的研究。他们将奎那克林的两个分子结合往一起,这使它在体外培养的细胞中的效力提高了10倍。
另一种疗法是应用可以抑制PrPSc形成的抗体在体外培养的细胞中达到抗PrPSc的作用。一些研究小组针对这一策略已经有了一些成功的应用。通过肠道给小鼠接种了朊病毒后,使用直接抗朊蛋白的抗体,延长了潜伏期。但是迄今为止,只有很少的一部分患者接受了抗朊病毒药物的治疗。奎那克林已成为变异性克-雅病和散发型、遗传性脘病毒病的口服用药。这种药并不能将他们治愈,但可以延长病程。我们期待进一步的研究证据。
临床医师也会让变异性克-雅病的患者使用木硫酸盐。这种药通常被用于治疗膀胱疾病,它的分子带大量电荷,不太可能通过血脑屏障,因此需将其直接注入脑室。这种药明显减慢了一位年轻男性变异性克-雅病患者的病程,但它似乎不太可能弥散至全脑,因为与它类似的带大量电荷的的药物通过同种的作用方式不能做到这点。
在我们对奎那克林及其它抗朊病毒药物的药效做出任何评价之前,首先需要一个临床对照试验。但有时候,即使是一期临床试验的结果都不足以说明什么问题,因为我们最初也许并不清楚药物在体内的代谢情况,也就无法确定如何给药才有效。比如说,许多治疗癌症的药物需要间歇给药,随着病程的变化给药或停药,以减低毒性。

虽然通向战胜朊病毒的道路看起来还很漫长,但是与5年前相比,我们还是向前迈进了一大步。同时,研究人员也希望,在人们发现朊病毒病的有效治疗方法时,这些方法同样能对其他的神经系统退行性疾病有效,包括老年性痴呆、帕金森氏病、脊髓侧索硬化症。因为上述的这些疾病都有异常的蛋白质积聚,所以通过朊病毒研究出来的结果可能也适用于这些疾病。
李逸、刘婷婷/译
王韵/审
曾少立/校
请 登录 发表评论