研究人员希望通过干扰日益扩展的癌肿血管网,来切断癌肿的基础支持系统。
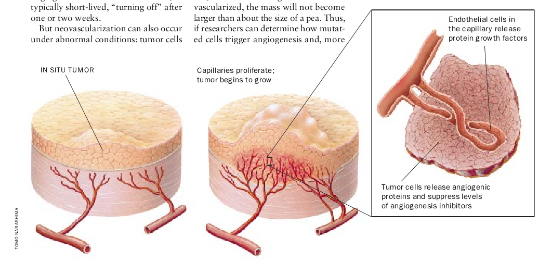
称为毛细血管的微细血管实际上贯穿着机体的所有组织,它们为机体组织补充养分,并带走废物。在大多数情况下,毛细血管的尺度和数量都不会增大,这是因为排列在这些窄细的血管内壁上的内皮细胞没有分裂的缘故。然而,有时——如在行经期间或机体组织受到损伤时,这些血管却开始迅速生长。这种称为血管生成的新的毛细血管增生现象一般说来持续的时间很短暂,往往在一两周之后便“停止”了。
然而血管生成在一些异常的情况下也会发生——癌细胞能够“开始”血管生成,随着新的血管带来新的养分和称为生长因子的蛋白质,癌肿便会长大。事实上新血管生成看来似乎是癌肿由小而无害的一团突变细胞转变成大而恶性生长且能扩散到体内其它器官中的组织的几个关键步骤之一。癌细胞最初在健康组织中产生时,通常都不能促使新血管生成而除非这恶变的细胞团有了新血管生成否则癌肿将不会长到比豌豆更大。因此若是研究人员能够弄清突变的癌细胞是如何导致新血管生成的并且对于患者来说更加重要的是,研究人员若是能够找到如何阻止这一过程的方法,他们就掌握一种归他们支配的强力新型抗癌疗法。此外,由于抗血管生成药物能够阻止新血管生长。却不会破坏健康血管,从理论上讲,这类药物不会损害为正常组织供血供氧的血管。(然而,血管生成抑制剂能使月经停止或延迟伤口愈合。)
几十年来对于血管生成对癌症发展的重要性的研究一直是实验室研究的一个极其重要的领域——笔者就曾在本世纪70年代中期写过一篇针对这一课题的早期研究的文章(参见《科学美国人》19768年5月号Judah Folkman所撰"The Vasculariation of Tumors"一文)。然而,只是在过去7年内这一研究才走出实验室而进入临床领域。1989年一种抗血管生成药α干扰素开始初次临床试用于治疗威胁生命的血管瘤(一种主要见于婴儿的良性血管瘤)。
到1992年,第一种用于癌症患者的抗血管生成药TNP-470(烟曲霉素的合成类似物)进入临床试用,最初的研究仅限于几种肿瘤,然而美国食品与药物管理局现已允许医生将TNP-470床试用于治疗各种各样的人类癌症。在过去4年里,至少还有另外7种抗血管生成剂开始临床试用于治疗晚期癌症,这些药物中的一种还试用于眼球血管生长异常的患者。 为了探索抗血管生成药的实际应用,许多研究人员作了多年努力,然而,遗憾的是,他们为数众多,而本文限于篇幅又无法一一列举。例如,在过去几年里,研究人员至少在人体内发现了14种不同的能够导致血管生成的蛋白质,此外还发现了其它几种能够阻止血管生成的蛋白质。最近研究人员发现,这些天然的血管生成抑制物之一在正常情况下受到抑癌基因P53的控制,而这种基因同各种癌症均有牵连。在有了这类线索的情况下,癌症研究人员继续提高对血管生成在肿瘤生长的作用以及对阻止血管生成的方法的认识。
血管生成是癌症扩散的必要条件
正如癌症发展的大多数方面的情况一样,血管生成扭曲了一种正常的生物学过程,此处即指对血管生成的调控过程。比头发丝还细的毛细血管的排列使得几乎体内的每一个健康细胞都能直接在毛细血管表面生存。若是一个健康的细胞变成了也细胞并开始迅速分裂,那么由此而产生的子代细胞便会以微观的团块累积起来。随着癌细胞的累积,它们离最近的毛细血管也就越来越远。当这些癌细胞累积到数百万个之多时,时常称为“原位癌肿”的细小肿瘤便不再长大并进人一种稳定的状态,在这种情况下,死亡的细胞与增生的细胞数量相等。癌肿之所以在这种情况下不再长大,部分原因在于癌细胞难以获得养分、蛋白质生长因子和氧。这些很小的癌肿若是长在皮肤或子宫预上。便有可能被觉察出来,然而若是长在乳腺、
肺部或结肠之中,则有可能在长达数年的时间里无所觉察。令人遗憾的是,我们至今还缺乏相应的技术,无法在内部器官的大多数原位癌肿尚很小时将其检查出来,而只能在用手术切除了该组织并用显微镜检查之后做到这一点。
在保持于这种稳定的状态数月甚或数年之后,原位癌肿有可能突然诱发新的毛细血管生长并开始侵袭其周围的组织,癌肿使天然生成的能促进新血管生成的蛋白质发挥作用。突变的癌细胞本身有可能产生大量的这类蛋白质,或者动用邻近的组织中的血管生成蛋白质,要不然就促使其它种类的细胞(如巨噬细胞)释放血管生成蛋白质。
然而,甚至有可能在利用了上述这些机制之后,癌细胞仍然无法导致血管生成。据西北大学诺埃尔·鲍克的研究小组以及加利福尼亚大学(旧金山)边格拉斯·哈纳亨的实验室最近发现,某些癌细胞够产生两种类型的蛋白质:一种能够促进血管生成,另一种则能抑制血管生成,两者之间的平衡决定着该癌肿是否能够导致血管生成。而实验结果表明,导致血管生成的能力极有可能取决于所产生的血管生成抑制蛋白质的数量是否减少,因此,事实上,促血管生成的癌细胞能够松开阻止新的毛细血管扩展的天然“刹车”,而一旦某个癌肿变成了促血管生成性的,它就往往会保持这种趋势。
一旦新血管开始形成了,许许多多的新的毛细血管就会会聚于该微细的癌肿,每根血管不久就会拥有厚厚一层迅速分裂的癌细胞。这些癌细胞中的一些并非促血管生成性的,然而却仍然是由邻近的细胞所聚集的毛细血管维持的。于是,癌肿便能迅速扩大了。在大约几个月的时间内,癌肿有可能长到1立方厘米大小,并拥有约10亿个癌细胞。
为了促使癌症进一步发展,新分裂的内皮细胞还会释放至少6种不同的能促使癌细胞增生或移动的蛋白质。例如,就乳腺癌而言,癌肿新生成的毛细血管的内皮细胞就能产生蛋白质白细胞介素-6,它能增大乳腺癌细胞离开癌肿,转移到血流中并扩散到其它器官,即癌症转移的可能性。一些转移的癌肿含有已是促血管生成性的因而能够迅速生长的细胞,然而,其它一些转移的癌肿则所含主要为非血管生成性的细胞——因而有可能休眠数年之久,要到原位癌肿受到治疗或被切除之后很久才变为血管生成性的。
癌肿发展到这一阶段时时常会引起一些能迅速得到鉴别的症状。出现在非行经期或小便、大便和痰中的血液表明,子宫颈、膀胱、结肠或肺部已分别有新血管生成。到乳腺癌已能从乳房X线照片上看出时,癌肿即已完成了新血管生成,伴随着卵巢癌出现的血红腹水,前列腺癌的骨痛症状,脑癌的脑部肿大以及常见于结肠癌的消化道阻塞皆起因于癌肿的新血管生成。日益扩大的癌肿所释放的生物学活性分子还有可能引起其它症状,如体重减轻和血凝块形成之类。
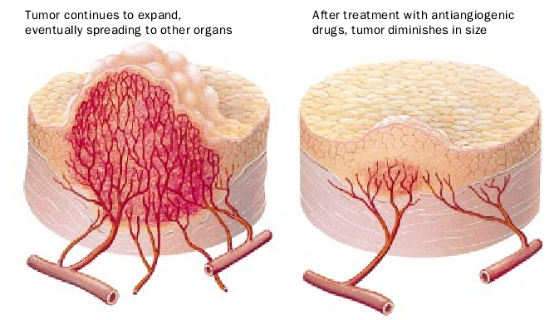
缩小癌肿
目前,诊断出任何一种癌症的患者一般都要依靠外科手术或放射性治疗来摘除或杀灭原位癌肿,并且还要依靠继续放疗或化疗或两者以消除体内遗留的任何癌细胞。与其它许多抗癌疗法不同的是,抗血骨生成疗法并非着力于杀灭癌肿,而是通过限制癌肿的供血,来努力缩小癌肿并防止其长大,抗血管生成剂使新血管无法在癌肿周围形成,并破坏掉为癌肿供血的现有的异常毛细血管网。目前,除了已在临床试用的一些抗血管生成剂以外,一些大学的实验室和全世界的约30家制药公司和生物技术公司还在研究许多可能的抗血管生成剂。
具体说来,正在研究的抗血管生成剂中,有两种抗血管生成的效力很强,这意味着它们最终将会成为高效癌症治疗剂。戴维. A. 切勒什(Cheresh)及其在斯克里普斯研究所的同事发现了这类药物中的第一种——一种干扰另一种称为整合因子(integrin)的分子的蛋白质,这种物质大量见于生长中的内皮细胞表面。若是整合因子(命名为“α-vβ3”)被阻断了,那么增生的内皮细胞便会死亡。
这类有希望的药物中的第二种即蛋白质“抗血管生成因子”(angiostatin)是由笔者在波士顿的儿童医院医学中心的实验室的迈克尔·S. 奥赖利在小鼠的尿液中发现的。在已知的血管生成抑制物中抗血管生成因子属效力最强之列。动物实验表明,它能阻止大癌肿或其转移癌肿中几乎所有的血管生长。被植入小鼠体内并允许长到小鼠体重1%大的人类前列腺癌,结肠癌和乳腺癌,用抗血管生成因子治疗后能缩小到显微尺度,并且只要持续给予抗血管生成因子,就能使这些癌肿继续保持在休眠状态。此外,抗血管生成因子的专一性很强它只阻止内皮细胞的增殖,而并不阻止其它细胞或处于正常休眠状态的内皮细胞的增殖。这种专一性有极大好处—研究人员尚未在实验动物中发现这种药物的任何毒副作用。此外,实验动物体内似乎没有产生对抗血管生成因子的耐药性。
抗血管生成因子实际上是比它更大的蛋白质血纤维蛋白溶酶原的片断,这种溶酶原本身其实并不是抗血管生成性的,事实上,有几种抗血管生成物蛋白质是较大的蛋白质的内部片断(例如,另一种抗血管生成物就是蛋白质促乳素的片断),这意味着正常的血管生成抑制物在某种意义上可能是储藏在较大的蛋白质之中的,因此,当人体必须停止正常的血管生成过程时(如伤口愈合后或排卵后),就只需要将较大的蛋白质分解,即可将这些天然的血管生成抑制物立即加以应用了。
提供治疗
实验室研究以及正在进行的血管生成抑制剂的临床试用为这些药物在得到美国食品与药物管理局的批准之后最终用于癌症患者提供了重要的准则。例如,血管生成抑制剂初步用于临床治疗时,极有可能是同目前的常规癌症疗法配合使用。设在波士顿的达纳-法伯癌症研究所的贝弗利·A. 泰克(Teicher)已通过动物实验证明,血管生成抑制剂和化疗剂配合使用比单独使用其中任何一种更为有效,在一项研究实例中,两种治疗剂配合使用治愈了42%的患癌动物,而单独使用其中任何一种治疗剂却未能获此效果。
这两种疗法明显的协同作用的一个可能的解释是,癌肿内的两种细胞——内皮细胞和癌细胞——对治疗的反应各不相同。例如,与癌细胞相比,内皮细胞的突变率很低甚或查不出来,因此通常不会变为耐药的。此外,每10到100个新的癌细胞需要至少一个新的内皮细胞。(1克癌肿含有约0.2亿内皮细胞及1亿至10亿癌细胞。)因此,当一种血管生成抑制剂阻止了一个内皮细胞的生长时其对癌细胞的效力会得到放大。
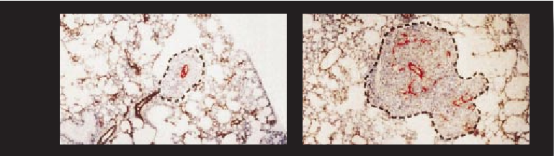
图1 血管生成(即新血管生成)涉及新血管增生,这一过程能将一小团通常无害的异常细胞(称为“原位肿瘤”)转变成一大块能向其它器官转移的癌肿。旨在干扰血管生成的药物如阻止血管生成蛋白质作用的药物,能够使癌肿缩小并有可能使之维持在休眠状态。
研究人员还把血管生成抑制物和放射疗法合在一起作了共同研究。起初对于放疗和血管生成抑制剂并用能否增进放疗的效果,肿瘤学家和放射学家之间曾有过争议。然而,泰克最近发现,对小鼠癌肿采用放疗和血管生成抑制剂合并治疗后,放疗的效果确实有所增强。目前,研究人员正在对动物作几种血管生成抑制剂(包括TNP-470和二甲胺四环素——抗生素四环素的一种相关物)和放疗的合用研究。
未来的方向
在常规的化疗或放疗完结之后,血管生成抑制剂有可能作为一种长期的抗癌疗法而得以应用。若是癌症已经转移,那就有可能需要作长期的抗血管生成治疗,在其它一些情况下,有可能短期使用抗血管生成剂,这或许是在用外科手术摘除一个大癌肿之前。为了维持癌症的休眠状态,还有可能用抗血管生成剂作周期性的治疗用药时间甚至可能长达数月或数年。值得庆幸的是,由于人体内对这类药物普遍缺乏抗药性以及这类药物毒性很低、使之可以长期使用。
尽管迄一今为止研究人员已对血管生成作了20多年的研究,但关于血管生成过程,它是如何受到调控的以及如何能在治疗上对它加以控制,却仍然留有许多问题。例如,至今无人知道,为何某些癌肿(尤其是宫颈癌)的新血管生成比其它一些癌症发生得早得多,并且尚在开发中的抗血管生成药也面临着所有临床试用共同面临的惯有的问题——有可能暴露出意料之外的副作用,或者是一种抗血管生成药对小鼠有效而对人却无效。
此外正如任何一种新药的情况一样,抗血管生成药也还面临着有待于克服的潜在经济障碍。许多抗血管生成剂不是新近才发现的蛋白质,就是其它类型的分子。化学研究人员现在必须找到大规模生产这类化合物的方法:这一生产过程有可能耗资高昂,然而,经验表明,抗血管生成药的价格理应随着时间的推移而降低。
尽管存在着这些障碍,但抗血管生成药仍有希望为我们现有的医疗手段提供一种新的抗癌疗法。由于抗血管生成药不大可能引起抗药性以及其副作用普遍较小它们有可能证明是效益重大的。抗血管生成药可能还可以用于治疗以异常血管生成为特征的其它一些疾病。这类疾病中包括糖尿病性视网膜病、黄斑变性以及新血管性青光眼——即存在异常血管增生并因此而毁掉视力的所有眼病。此外,抗血管生成药治疗可能还能治好牛皮癣关节炎,血管瘤以及其它一些良性肿瘤。于是,抗血管生成药显然有着令人振奋的潜力——除了用于癌症,还可能用于多种严重疾病的治疗。
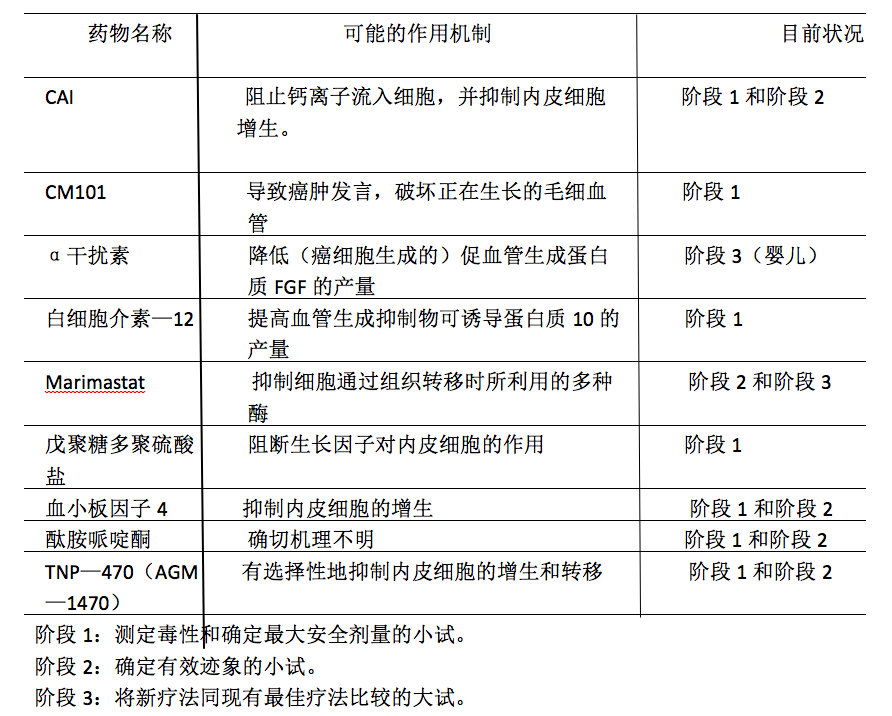
临床试用的血管生成抑制剂
尽管尚无任何血管生成抑制剂获准用于癌症患者,但已有许多这类药物目前在作临床试用。
(郑小石 译 王世德 校)
请 登录 发表评论