人类的遗传密码大约由30亿个DNA碱基组成但是仅仅10—15%的碱基组成基因和制造蛋白质的蓝本细胞人类与许多其它有机体的其余碱基序列的部分执行关键性的功能,如像帮助“接通”与“断开”基因,将染色体保持在一起但是许多DNA似乎完全没有明显的目的,结果导致一些人把它看作是“废物”部分。这种“废物DNA”包括称为DNA随体的奇特区域,它们是由4个DNA碱基——腺嘌呤(A),胞嘧啶(C),乌嘌呤(G)与胸腺嘧啶(T)——的各种组合构成的重复序列,重复了又重复就象遗传性口吃一样。
在过去几年中,研究人员开始发现,那些含有最短的重复序列的所谓微随体其重要性之大与它们的尺寸不成比例并且执行各种惊人的功能,的确,科学家们正在发现,微随体的重复性使它们特别易于生长或缩短度,并且这些变化对拥有它们的有机体既有好的结果又有坏的结果例如,在某些致病的细菌中,这些重复序列促进了可以使这些微生物在环境潜在的致命变化中幸存下来的新特性的出现一些微随体也可能对人类产生重大影响。因为至少有l0万个微随体发生在人的组和人类细胞的I)NA完全补体中——虽然迄今赋予人的微随体的唯一功能是消极的——引起各种各样的神经疾病——但是微随体可能是有助于形成现代人类的进化过程残存下来的残遗体。
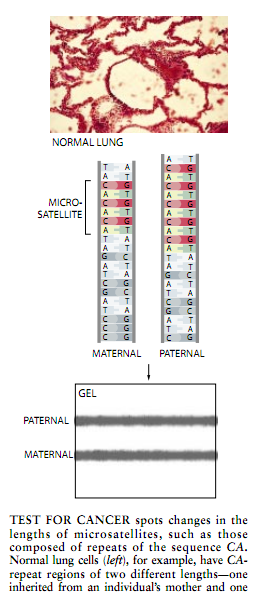
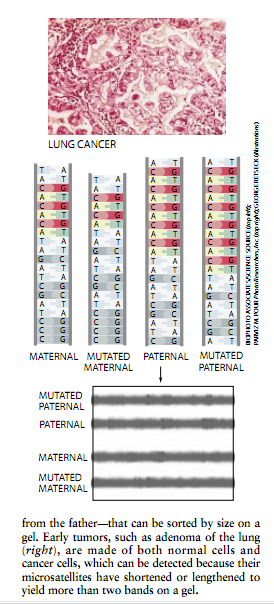
正当一些研究人员寻找人类载有这样多的重复DNA的原因时,现在许多人正在研究利用微随体来诊断神经疾病与识别患有这些疾病的人他们还发现在一些癌症发生的早期,微随体长度有变化,这使它们成为早期癌症检测的有用标记。因为微随体的长度因人而异科学家们甚至已经开始用它们来识别罪犯与确定父亲的身分——也就是所谓DNA轮廓法或“指纹法”。
在20世纪60年代首先鉴定出微随体DNA研究人员发现,当他们在某些条件下离心DNA时,它沉淀为两层或两层以上:含有基因的一条主带与开始被称为随体措的副带这种随体带原来是由很长的重复DNA序列构成的在1985年,莱斯特大学的Alec J. Jeffreys发现了DNA的其它的,较短的重复区域,他将其叫做小随体,这些小随体原来是由15个或更多的碱基的拷贝组成的。
Jeffreys及其同事也确定了在一个指定的小随体中的拷贝数目在个体间有所不同(这一发现使他们发明了DNA指纹法)。在本世纪80年代后期,在威斯康星州马什菲尔德的马什德医学研究基金会的James L Weber与Paula L. May和俄勒冈卫生科学大学的Jeffrey A Luty分离由更短的DNA拷贝构成的随体,并且将它们命名为微随体:这些也将证明对DNA指纹法是有用的。
今天,科学家们普遍认为,微随体DNA由多达6个碱基组成,它们重复又重复,并且端部对着端部,就像由同类型的车厢组成的一列火车使微随体DNA对进化来说显得如此重要的是它的极其高的突变率它可能从一代至下一代得到或失去复制的突变率比基因(如导致镰状细胞贫血的基因)发生致病单碱基突变大1000倍,虽然导致镰状细胞贫血的单碱基突变很少突变回良性状态,但微随体能够容易地在几代内恢复到以前的长度。
“灵巧的”微生物
微随体在病原细菌的多样性中的作用是l986年在蒂宾根马科斯普朗生物研究所的Thomas F Meyer的实验室中发现的。Meyer及其同事当时正在研究能够引起性传播疾病(淋病)的细菌一一淋病奈氏球茁(Neisseria gonorrhocsa),该细菌是一种单细胞有机体,具有多达12种由叫做Opas基因编码的外膜蛋白质。(基因的名字来自于制造Opas蛋白质的细菌群落的不透明的外观)由0I}aS产生的蛋白质之所以重要足因为它们让细茁粘附到与侵入上皮细胞,如构成吸道的细胞及免疫细胞,(称为吞噬细胞)每个Opas基因都含有由5一碱基彩带CTCTT的多个拷贝组成的微随体。

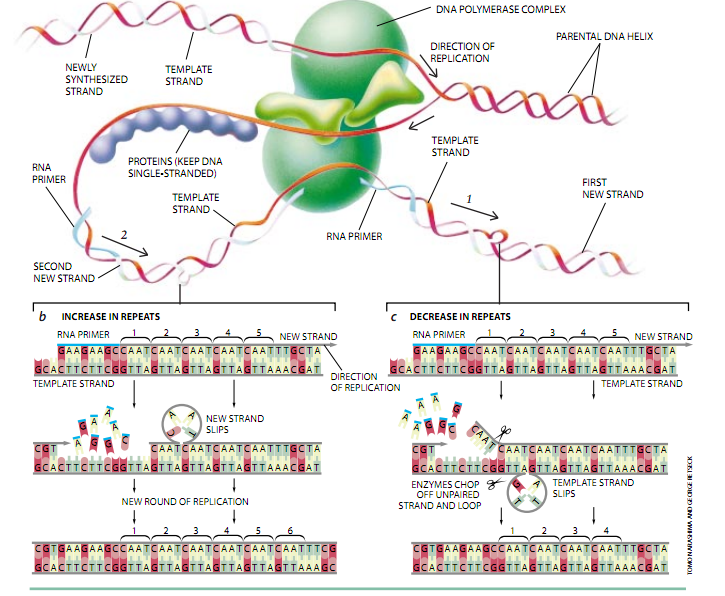
由微随体重复传送的极大变异源自这样的事实:重复特别易于发生DNA复制错误经常是通过所谓的滑脱链配对错误而发生的在细胞——细菌或其它生物的——能复制以前,它必须制造一套它的DNA拷贝制这是一个复杂的过程,因为每个DNA分子都是一个类似扭曲的梯子的双螺旋构型,其中梯子的横档是碱基对它的遗传代码则是由梯子每一边上的碱基读出来的:它与另一边上的碱基是互补的(A总是与T配对,G与C配对)。
在DNA复制期间,梯子沿中间裂开,从而分开碱基对象称为DNA聚合酶的酶拷贝每条链一样当制造新股时,它与其模板配对当老的模板股或新形成的互补滑脱并与其它股上的错误重复配对时,滑脱的错误配对可能发生这样的滑移使DNA聚合酶加上或消去DNA新股重复中的一个或更多个拷贝。
这样的滑移机理的频率在N. gonorrhoeae中是很高的:细菌每次分裂时、大约每100至1000个子细胞就有1个将带有一个改变CTCTT重复的突变。这种改变可能对Opas基因有引人注目的影响,因为遗传信息是三个碱基中的“字”(叫作密码子)读出的蛋白质是氨基酸串,并且每个密码子确定蛋白质链中的一个特定的氨基酸。因为重复没有3个碱基长,重复数目的增加或减少都会改变所有后来的密码子的含意。
就Opas基因而论,消去一个CTCTT导致被缩短的与不能粘附到寄主细胞的蛋白质的产生:从而,携带有缩短了的蛋白质的细菌不能进入那些细胞。但是随后的滑移有一次好的机会把重复加回去,让Opas基因又一次产生功能性蛋白质这一称为阶段变化的可逆转换,是在许多致病细菌中发现的通过打开或者关闭一代到下一代的各种基因N. gonorrhoeae能够增加其存活的机会。例如,有时候附着到寄主细胞或进入寄主细胞就像细菌传播到新寄主一样对微生物有益;在其它时候,不和寄主细胞——特别是吞噬细胞——发生反应在策略上对细菌更有利,因为这些细胞会吞投与消灭细菌。
滑脱股误配对细菌改变其表面分子的能力的意义也在流感嗜血菌(Hemophilus influcnzae)中作了广泛的研究,这种细菌的b型品系是危及生命的大脑侵染细菌性脑膜炎的主要病原。在本世纪80年代后期疫苗出现以前,每750个年龄小于5岁的儿童中大约一个感染过H. influcnzae脑膜炎。
H. influenzae的外膜布满了脂肪与糖的分子,而脂肪与糖则联合在一起产生称为脂多糖(LPS)的分子LPS的一部分称为磷酸胆碱它有助于H . influcnzae粘附到人的鼻子与咽喉中,细菌在那里正常生活而没有引起症状制造LPS所需要的基因至少有3个含有4一碱基序列CAAT制造的微随体,因为这一点适用于N. gonorrhoeae的Opas基因的微随体,所以在这些基因中CAAT重复数目的改变能够使H. influcnzae制造具有或没有磷酸胆碱的LPS。
宾夕法尼亚大学的Jeffery N. Weiser证明在其LPS分子上具有磷酸胆碱的H. influcnzae品系I一所谓的ChoP+品系——比没有它们的品系(称为ChoP+品系)能更有效地聚生在人的鼻子与咽喉中但是没有ChoP+的细菌对存在于寄主血液与其它组织液中的各种因素更具有抗杀伤性。细菌细胞能移在两种状态问转变这取决于它们在呼吸道中处不受干扰地生长的状态,否则它们就通过血液传播到其它部位因为呼吸道里它们可能受免疫系统组成部分的攻击。
从人类中分离出的大部分。
H. influenzae细菌都是ChoP+变种它们对免疫攻击是敏感的。ChoP+变种不可避免地通过滑脱股误配对产生,但是它们通常并不持续留在呼吸道内。因为它们不像ChoP+品系那样有效地附着于寄主细胞,但是如果寄主发生了使鼻组织发炎的病毒感染,炎症就能够增加细菌接触寄主免疫系统中的防御蛋白质的机会。在这种情况下ChoP+变种就会有有利条件,因为它们能够避开这种攻击。一旦病毒感染减速,由微随体DNA的进一步滑脱股误配对产生的ChoP+突变将又一次占优势。这些可以很容易换上或换下的基因已经因为它们至少能使一定群体中的一些细菌适应新环境的偶然事故而被命名为偶然事故基因(Contingency gene)。由偶然事故基因编码的特征多样性包括免疫系统的控制识别一般性的能动性向化学信号运动(趋化性)、对寄主细胞的附着与侵入,对营养物的获取与对抗生索的敏感性偶然事故基因占细菌DNA的很小部分,但是它们能对功能作用提供极大的灵活性。例如,如果在典型细菌的2000个基因中只有l0个偶然事故基因,细菌就能够呈现210——1024种——不同的“换上”与“换下”基因组合这种多样性确保在一个群体中至少有一个细菌能够经受住寄主免疫或基它防御机制,从而能够复制产生繁荣旺盛的新群落。
引起疾病——杀死给予生命的寄主可能结果适得其反——也许是细菌能够产生这么多变种所付出的代价之一。偶然性变种可能使其偏离在寄主中的生态位。例如,它可以渗入呼吸道或肠道的衬里细龅,在身体的其它部分产生可能致命侵染但是倘如这样的事件很少发生偶然事故基因对细菌种类活的好处就会胜过杀死某些寄主的不利之处这些基固的微随体是真正的进化适应偶然发生的这种异常的重复是难以置信的:它们必定因其能使细胞群体迅速适应环境变化而进化并被保存下来了。
人类微随体
尽管偶然事故基因有用,但它们显然局限于细菌微随休的作用似乎与象我们自己这样的真棱机体不相同,真核有机体的细胞含有核迄兮鉴别的真核微随体没有一种看来要争夺DNA被读出的路径与产生非功能性蛋白质它们大部分存在于基因之外,但是约有10%实际上落在它们之内,这10%,几乎是所谓的三联体重复并且往往以3个碱基为单位扩大或收缩就像在一个句子中加入或减少一个“and”或“the”几乎不会使它的意义模糊不清那样,三联体的重复可扩大或收缩而干扰基信息因为具有与密码子相同的长度,蛇们可以仅仅导致插入与除去一些重复氨基酸而不改变沿着线路的所有其他氨基酸的重复序列。
那么,微随体在高等动物中的功能是什么呢?科学家们推测,至少它们中的一些必定有用处,因为真核生物必定比细菌有更多的微随体,并且它们中的许多碰巧在与调节基本细胞过程的通路有关的基因中或其附近。但是,这些作用可能是什么仅仅出现了一点线索。
现在已被跟踪到的真核生物微随体的少数影响通常是有害的。例如,危险的神经变性疾病亨廷顿舞蹈病——特点是痴呆晚发作与运动原控制逐渐丧失——是由为尚不知其功能的大蛋白质Huntingon编码之基因的缺陷型所触发的。正常基因含有一个长的,三个一组的重复微随体,这个微随体在蛋白质的开始处附近加上一列称为谷氨酰胺的氨基酸。
现在已经知道是多种这样的三联体-重复病,他们大部分是罕见的神经性疾病,引起这种病的微随体重复约有一般位于基因内部,并且大部分编码谷氨酰胺。其余的十分靠近他们能够影响其功能的附近基因。
这些罕见的神经性疾病之一——脊柱延髓肌肉萎缩——起因于X染色体上基因内微随体的膨胀:基因编码雄激素的受体。在其雄激素受体基因之一的部分中具有40个或更多三联体重复的人发生此病。
雄性激素受体的重复太少也可能有不适宜的影响,其他几个研究小组证明了,具有23个或更少重复的男人则有前列腺癌增加的危险,但是这样的情况是罕见的。
逐渐形成的进化
惊人的是,这么多的人类三联体重复病涉及到神经功能,并且这些与人类三联体重复有关的疾病还没有一种在其他灵长目中被报导过。如果这样的疾病证明是人类独有的,它们可能表示人类由于大脑的迅速演化而付出的遗传代价。
1989年,作者之一(Wills)根据理论基础假设,有些基因使演化的能力得到发展。按照这一假设,在一某些可预测方式变动的环境中——如像变得较暖和或校凉冷——具有迅速演化的遗传器官会有优势,细菌的偶然基因证明是进化基因的绝好范例。也许真核生物的微随体形势比细菌的偶然基因提供的那种形式的调节更微妙。在人类中,业已发现基因内的微随体影响从胆汁色素胆红素到神经递质等蛋白质数目的产生率,它们是在神经细胞间携带信息的化合物。
苏黎世大学的Walter Schaffner及其同事实际上证明了,在抑制基因的开端加上可为谷氨酰胺或脯氨酸序列编码的微随体,能够增加其产生蛋白质的能力,也许它的破坏性比偶然基因开关少这样多,所以这种形式的基因调节作用出现在复杂得多细胞有机体的进化期间。
科学家仅仅开始探索微随体在人类自身中的作用。也许能够在数目有限的状态中迅速转换的重复讲帮助我们洞察自己适应环境变化的能力,就像偶然基因在细菌中所起的作用那样。
请 登录 发表评论