精神疾病的大脑开关
生活经历能以出人意料的方式引发精神疾病:不需要改变基因本身,只通过“表观遗传”的修饰来打开或关闭基因。
撰文 埃里克·J·内斯特勒(Eric J. Nestler) 翻译 李凌宇
刚开始,他还可以正常生活——按时上课并且与朋友们保持联系。但是很快,毒品占据了他的生活。格雷格辍学了,开始在快餐店或者连锁店打零工。他在一个工作岗位上极少坚持超过一两个月,不是因为消极怠工,就是因为和顾客以及同事争吵而被开除。他的行为变得越来越古怪,有时还会很暴力,他为了满足毒瘾而偷窃,导致多次被捕。多次戒毒的尝试都以失败而告终。
到了格雷格三十三岁,法院把他送去精神病院做评估的时候,他过着穷困潦倒、无家可归的生活,他已经被家庭抛弃,成为毒品的囚徒。
是什么使得格雷格无法抗拒可卡因的诱惑,以致毁掉自己的一生呢?而跟他拥有相同基因的双胞胎兄弟,又是如何逃脱了相似的命运?为什么某些人一辈子都会沉溺在毒品中,而另外一些人却可以摆脱年少轻狂所犯的错误,在人生中有所建树呢?
这些问题已然是老生常谈,而神经科学家正在尝试用一种全新的方法来寻找问题的答案,这种方法得益于其他领域的发现。在过去十年当中,研究胚胎发育和癌症的生物学家发现了一系列备受关注的分子机制,它们让外部环境不需要改变基因本身所包含的信息,就可以影响基因的表达。与基因突变不同,这些“表观遗传”的修饰标记改变了基因表达的活性。某些情况下,这些修饰会伴随一生。
目前,我的实验室以及这个领域中的其他实验室正发现种种迹象,表明吸毒或慢性应激引起的表观遗传修饰会改变大脑对生活经历的反应方式:它可以决定一个人能够迅速戒毒还是面对毒瘾不能自拔、或会患上抑郁症或者其他一系列精神疾病。对于这种基因与环境之间在分子层面上强大的相互作用,我们目前还知之甚少。但是,我们希望我们的研究会促进针对一些痼疾的有效治疗,甚至还可能会对精神疾病的遗传机理提出新的见解。
基因之外
过去几十年,对成瘾、抑郁症、孤独症、精神分裂症以及其他一些神经紊乱疾病的研究,主要关注造成这些疾病的基因根源,而我们现在正努力去弄清楚表观遗传对精神疾病的影响,这将会填补过去的研究所留下的空白。
像很多常见疾病一样,这些让人备受折磨的精神疾病具有高度遗传性:大约一半的成瘾及抑郁症是有遗传性的,这比高血压或者大多数癌症的遗传风险要高得多。但是,基因并不能解释一切。就像我们从格雷格与马特的例子中所看到的,即使拥有相同的基因,也不能保证两个人会患相同的病。对于那些在基因型上易患精神紊乱的人群来讲,环境刺激往往会增加发病风险,比如接触毒品、承受压力,甚至包括在发育过程中偶然的分子事件。没有哪两个人会经历一模一样的外界刺激及发育过程。
那么问题就变成了,这些外界刺激是通过什么机制引发精神疾病的?从某个层次上来讲,答案是显而易见的:遗传和环境的作用都会影响到大脑中的神经细胞。神经细胞处理着我们经历的所有事情,不管是看电影、拥抱、吸可卡因,还是考虑晚饭吃什么,神经细胞之间通过释放和识别一些被称为神经递质的化学物质来交流信息。神经递质可以激活或者抑制某些神经细胞,也可以控制一系列基因的活性。那些被特定神经递质影响的基因会决定神经细胞如何响应外界刺激,最终影响人的行为方式。
这些影响一般持续时间较短。例如,注射可卡因会激活大脑中的奖赏回路,从而引发暂时的愉悦感。这种感觉会很快消褪,神经系统会自己重新调整回原来的状态。至于毒品、压力或者其他经历如何造成长期影响,使得一个人患上抑郁症或者成瘾,却还是一个谜。很多神经科学家认为这恰恰可以用表观遗传来解释。
经验的痕迹
要理解表观遗传为什么这么重要,就需要了解一下基因活性是如何被调控的。一个基因,简单来说,就是一段脱氧核糖核酸(DNA),它可以指导生成某一特定的蛋白质;蛋白质执行着细胞中大部分的功能,从而操控着细胞的行为。DNA不是随随便便被塞进细胞核里的。相反,它缠绕在一簇叫做组蛋白的蛋白质上,如同缠在线轴上的线,然后再进一步缠绕成染色体。染色体中蛋白质和DNA的复合物就是染色质。
包装DNA不仅仅是为了让细胞核井然有序,也有助于调控被包裹在里面的基因的活性。比较紧密的包装往往将基因维持在非活化状态,因为这样一来那些使基因活化的分子便无法靠近。比如说,在神经细胞中,那些编码肝脏中的酶的基因就被藏在紧密包裹的染色体区域。
然而,当机体需要一个基因的时候,它所在的那段DNA区域就会略微展开,使得这个基因能够接触到细胞中负责将DNA转录成RNA的分子。在大多数情况下,RNA会作为合成所编码的蛋白的模板。例如,某些基因负责编码神经递质,则刺激一个神经元,就可能会使细胞提高这类基因的转录水平,从而合成更多的神经递质。
一段染色质是松散(预备活化)还是高度压缩(永久或暂时性关闭),都会受到表观遗传标记的影响。表观遗传标记是指添加在组蛋白或者DNA上的化学标签。这些标签有多种不同的形式,它们一起构成某种代码,指示该基因是否应该被转录,以及这段染色质应该被包装得多紧(见右图)。一个基因活化程度的强弱,取决于它的染色质是如何被标记的。
表观遗传修饰由多种酶参与,其中一些酶负责添加化学分子标记,还有一些负责移除标记。洛克菲勒大学的C·戴维·阿利斯(C. David Allis)是这一领域中的领头人物,他将这些酶比作表观遗传代码的“写作者”和“橡皮擦”。例如,组蛋白乙酰转移酶将一个乙酰基团连接到组蛋白上,它就是一个“写作者”;组蛋白脱乙酰基酶清除了这个标记,它则是一个“橡皮擦”。
这些标记还会吸引其他蛋白质过来成为“阅读者”。阅读者识别特定的表观遗传标签,然后通过招募其他的调节蛋白使得标签附近的染色质展开或紧缩,这些调节蛋白可以激活或抑制该染色质中基因的转录。比如说,高度乙酰化的组蛋白吸引趋向于打开染色质的“阅读者”,以及其他一些增强基因活性的蛋白质。相反,携带有大量甲基化修饰的组蛋白会根据甲基化标记的具体位置,吸引抑制或激活转录的“阅读者”。
外界环境可以通过调控表观遗传“写作者”和“橡皮擦”的行为,也就是通过在染色质上贴标签和重新组织染色质,来影响基因活性。有时候这些标记只维持较短的时间,比方说,通过一阵持续地释放神经递质,让神经细胞迅速响应强烈的刺激。某些标记往往会存在几个月、几年,甚至一生,比如说有些标记,它们一直在起着加强或减弱参与记忆存储的神经连接的作用。
因此,添加或者移除乙酰化和甲基化基团以及很多其他标记,可以帮助大脑响应和适应来自外界环境的挑战及经历。我们和其他实验室在动物实验中刚刚发现,在成瘾和抑郁的情况下,那些对动物有益的表观遗传活动往往会出错,正常的表观遗传修饰被打乱,会激发欲望,造成挫败感,或者使实验动物长期表现出适应不良的行为。对人类尸体的脑组织进行的检测表明,以上发现可能同样适用于人类。
成瘾的导火索
与成瘾相关的发现,建立在过去研究的基础上,这些研究揭示了滥用药物如何挟持大脑天然的奖赏回路。例如很多研究已经发现,在可卡因、鸦片或其他成瘾性药物的刺激之下,基因的活化程度发生了大规模的改变。某些基因表达的改变甚至在戒毒后几个月仍然存在,研究者们亟须找到造成这种持续作用的机制。
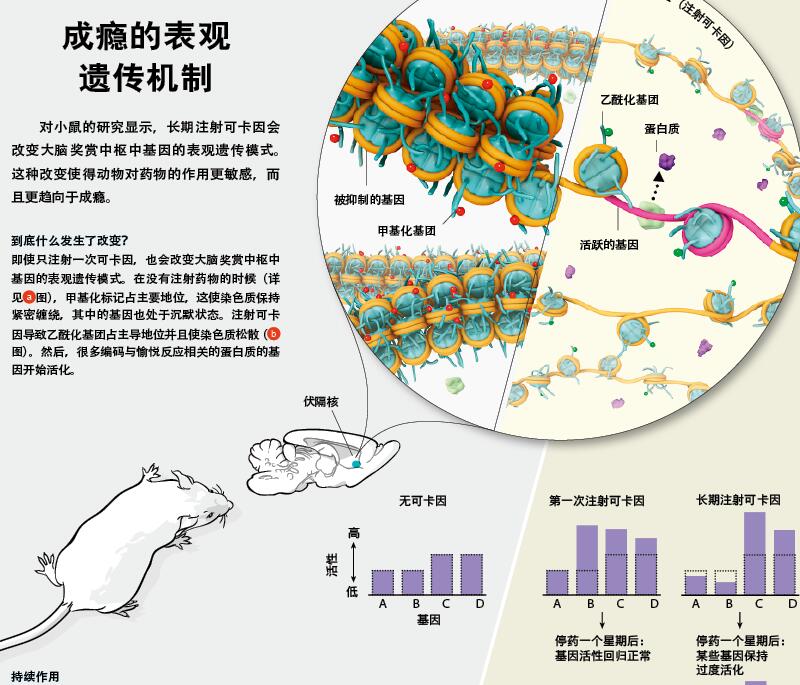
基于表观遗传的改变可以产生长时间的影响,大约在十年前,我的实验室开始着手检测可卡因是否可以通过改变表观遗传标记,来改变大脑奖赏中枢的基因活性。可卡因是一种很强的药物,它可以让动物成瘾,就像对人类一样。因此在实验室里,可卡因的长期影响相对容易被研究。
通过检测信使RNA的浓度——这是反映基因活性的直接指标,我们确认单次注射可卡因会引起显著而广泛的基因表达上的改变。小鼠在接受完第一次可卡因注射后一个小时,有将近一百个基因被启动。更有意思的是长期给药所发生的事情。有几个在单次给药时被打开的基因,在每天给药的情况下开始趋于沉默——连续给药让这些基因变得对药物不敏感。
然而,更多的基因与此截然相反:在第一次注射可卡因时这些基因被暂时性活化,而长期给药又进一步提高了它们的活化程度。有时候,在停止注射几个星期后它们依然可以维持活化。不仅如此,这些基因在动物停药一段时间以后依然对可卡因保持高度敏感。这样,长期给药就为这些基因在将来的活化埋下了伏笔,实质上就是让这些基因“记住”药物引起的报偿作用。这会让动物药瘾复发,从而为成瘾铺平道路。这种被提高的敏感性正源于基因的表观遗传修饰。
通过运用强大的技术手段对小鼠整个基因组的表观遗传标记进行分类整理,我们已经能够证明,长期注射可卡因会选择性地对大脑奖赏中枢的几百个基因的乙酰化和甲基化标记进行重组。总的来说,这些改变趋向于使染色质结构变得疏松,从而使得这些基因在下一次接触可卡因时更容易活化。这其中的许多改变是暂时性的,在动物接受药物后只维持几个小时。但是,有些改变持续的时间则长得多,我们已经记录到某些改变,它们至少可以持续一个月,接下来我们准备观察能持续更长时间的改变。
我们也逐渐开始理解导致这些持续改变的分子机制。我们发现长期使用可卡因抑制了某些用于移除乙酰化基团的“橡皮擦”的活性,同时还抑制了负责添加抑制性甲基化基团的“写作者”的活性。染色质的乙酰化程度越高,或甲基化程度越低,它的状态就会越松散、开放,从而使其中的基因越发容易活化。长期接触可卡因还会影响大脑奖赏中枢的其他“写作者”和“橡皮擦”的活性,在这之后,便形成了一系列有利于基因活化的表观遗传标记。支持这一观测结果的是,我们发现人为调整这些“写作者”和“橡皮擦”的活性,即使实际上没有给药,也可以模拟可卡因的效果,我们使实验动物对可卡因变得更敏感,更容易产生快感,这是成瘾的特点之一。
长期使用可卡因引起的“写作者”和“橡皮擦”活性的改变也可以持续很长时间,这可能是被标记的基因活性发生长时程改变的原因,也正是通过这种方式,实验动物会对未来一段时间内的刺激产生响应。大脑奖赏中枢可以对包括吃饭、性行为等广泛的刺激类型产生反应,改变这个回路中神经元的活性可以从根本上改变动物的行为模式。
抑郁症的标记
神经的适应性可以影响长期的行为方式,也可以用来解释一种延续时间最长、使人虚弱不堪、且较为常见的精神疾病:抑郁症。就像成瘾一样,这种疾病的各个方面都很容易通过动物实验来研究。在我的实验室,我们使用一种长期在社交上很挫败的小鼠模型做研究。我们将性格温顺的雄性小鼠与富有攻击性的小鼠成对养在一起。
经过十天的担惊受怕,温顺的小鼠显现出人类抑郁症的很多特征:它们不再对消遣玩乐(甜品,性行为)感兴趣,开始变得焦虑、孤僻、胆小,它们甚至过量饮食变得肥胖。其中的一些改变会持续几个月,并且可以通过长期服用人类使用的抗抑郁药物而得到好转。
仔细观察小鼠的DNA,我们发现在大脑奖赏中枢有大约2 000个基因的表观遗传修饰发生了改变。在其中的1 200个基因中,我们检测到一种特殊的表观遗传标记的增加,那就是抑制基因活化的组蛋白甲基化修饰。如此看来,抑郁症可以关闭一些关键的基因,这些基因的功能是激活大脑中可以让动物产生快感的部位,于是就造成了某种“分子疤痕”。我们发现,许多由精神压力引发的改变可以通过让动物服用丙咪嗪——一种广泛使用的抗抑郁药物,而得到逆转。在患有抑郁症的死亡病人的脑组织中,我们也已经检测到了相似的表观遗传改变。
尽管抑郁症在人类群体中是一个常见的疾病,但是并非每个人患抑郁症的风险都一样大。我们发现小鼠也是这样。在每天接受一次同类排挤的雄性小鼠中,大约有三分之一表现出对抑郁症的抵抗力:尽管它们同样遭受持续不断的压力,却没有像那些容易受影响的小鼠那样表现出消沉和倦怠。
这种抵抗力涉及小鼠的基因层面。在易患抑郁症的小鼠中观察到的许多由压力引发的表观遗传改变,在适应力强的小鼠中没有发生。不仅如此,适应力强的小鼠大脑奖赏中枢还有一系列基因被表观遗传修饰,而患抑郁症的小鼠,同类基因却没有经受这样的修饰。这一发现意味着,这套不一样的表观遗传修饰有保护作用,小鼠良好的适应性不仅仅是因为没有易感性,而且涉及一种主动的表观遗传机制,这个机制可以用来抵抗长期的精神压力。
我们还发现在适应力强的小鼠中被表观遗传修饰的具有保护作用的那些基因,恰恰是患抑郁症小鼠接受丙咪嗪治疗之后活性得到恢复的基因。我们知道其中一部分基因可以促进大脑奖赏中枢的活性,因此可以避免抑郁。这些观察结果提出这样一种可能性,在人类中,抗抑郁药物可能部分是通过活化一些具有保护作用的表观遗传机制来起作用的,正是这个机制让另一些个体天生对抑郁症有抵抗力。如果是这样,我们不仅要寻找可以消除慢性压力所带来的不良影响的药物,还应该找出能够促进大脑天然抵抗力的药物。
母亲的遗产
到目前为止,我所讨论的表观遗传的影响可以持续一个月,这是我们已经研究过的最长的时间段。但是,加拿大麦吉尔大学的迈克尔·米尼(Michael Meaney)和同事们证明,表观遗传修饰可以促进维持一生的行为改变。米尼研究了母亲的照料对表观遗传修饰和对下一代随后的行为所造成的影响。
研究者们知道,有一些母鼠可以表现出高层次的育儿行为,比如舔舐幼崽,给它们梳理毛发。而其他的母鼠却没有这么贴心。勤劳母鼠的后代与懒惰的母鼠养育的后代相比,表现得没那么容易焦虑,在受到惊扰的情况下产生的应激荷尔蒙也比较少。不仅如此,由善于照料幼崽的母鼠带大的母鼠,将来也会变成一个细心的母亲。
米尼的研究小组进一步揭示了,母亲的行为所产生的影响至少一部分是通过表观遗传机制来介导的。与经常得到呵护的幼崽相比,懒惰的母亲养育的幼崽在一个编码糖皮质激素受体的基因的调节序列上,有更多的DNA产生了甲基化修饰,糖皮质激素受体是一种存在于身体大部分细胞中的蛋白质。用来介导动物对应激荷尔蒙——皮质醇的响应。
在大脑中与学习和记忆相关的部位——海马体中,有检测到这种过多的甲基化修饰,它们会引起神经细胞产生更少的受体。因为海马体组织中,糖皮质激素受体的活化实际上是给身体发出信号,要求减少皮质醇的生产,表观遗传修饰让受体数目减少,加剧了动物对压力的反应,使得它们更加焦虑和恐惧,这些特征会伴随它们一生。
对糖皮质激素受体的影响也许只是整个故事的一部分。哥伦比亚大学的弗朗西斯·香巴尼(Frances Champagne)及她的同事在分别由勤劳母鼠和懒惰母鼠养育的两类幼崽中发现,编码雌激素受体的基因的表观遗传修饰也存在类似的差别。那么可能还有很多其他基因的表观遗传修饰最终会涉及对一些复杂行为的反应,比如母性行为,并且可以遗传。
在这种情况下,上一代在某个基因上发生的表观遗传改变可以有效地传给下一代,即使这些改变不通过生殖细胞来传递。母亲的行为可以改变幼崽大脑中基因的表观遗传调节,而幼崽长大后会表现出同样的行为,这又改变了它的幼崽的表观遗传标记和行为,从而流传下去。
表观遗传疗法
根据我们对表观遗传修饰和行为的研究来开发出更好疗法,治疗各类精神紊乱疾病,这将是未来几十年的一个重大挑战。比如说,我们及其他实验室已经找到可以保持组蛋白乙酰化修饰的药物,这类药物通过抑制擦除乙酰化标记的酶来起作用,具有显著的抗抑郁效果。
此外,尽管消极的育儿方式与DNA甲基化改变相关,米尼已经发现,同样的药物可以促进母亲的育儿行为(因为上调的乙酰化水平可以抵消掉过多甲基化带来的压制效果)。
虽然结果看起来很理想,但是目前市场上销售的抑制性药物对亢奋型的精神疾病可能不太管用。乙酰基的“橡皮擦”——组蛋白脱乙酰基酶,会在大脑和全身的细胞中负责调节表观遗传标记,因此,不加区别地破坏酶活性的药物有严重的副作用和毒性。一种可供选择的办法是生产某种药物,它们可以选择性地抑制特定类型的组蛋白脱乙酰基酶,这种酶富集在受某种精神疾病侵害最严重的大脑区域,例如奖赏中枢等位置。另外一个选择就是,在大脑中找出新的与表观遗传修饰相关的蛋白质。不过最有成效的方法可能还是先确定哪些基因在抑郁症或成瘾中会产生表观遗传修饰,比方说编码特殊的神经递质受体或信号蛋白的基因,它们都在神经细胞活化中起作用。然后我们可以集中精力来设计针对这些特定基因的活动的药物,或者直接研制以这些基因的蛋白质产物为标靶的药物。
表观遗传的传递
一个亟待回答的有趣问题是:与精神疾病相关的表观遗传改变在多大程度上可以遗传?在米尼的实验室,大鼠可以从它们的母亲那里“继承”母性行为模式和相关的表观遗传模式。但是,这些发生在大脑中的改变是被行为直接影响的,它们不通过生殖细胞中的基因标记来传递。因此,一个更具启发性的问题是:这样的经历会引发精子和卵细胞中的表观遗传改变,而后直接传给后代吗?
当然,怀疑滥用药物或长期压力会改变精子或卵细胞内基因活性的想法并不过分:毕竟,药物和应激荷尔蒙不仅仅局限在大脑,它们随着血液循环分布到身体各处,其中包括睾丸和卵巢。
而难以理解的是,生殖细胞中发生的这种改变如何遗传给下一代。当细胞发生减数分裂形成精子和卵细胞的时候,后天获得的表观遗传修饰会被消除。并且,就算这种改变在胚胎中存在,它们如何做到在成体中只影响大脑个别区域,或者只影响内分泌器官中的基因活性?
虽然难以理解,但还是有一些耐人寻味的研究提示,某些表观遗传修饰是可以遗传的。几个研究团队已经发现,长期承受压力的啮齿类动物生出来的后代对压力异常敏感。例如,瑞士苏黎世大学的伊莎贝拉·曼苏(Isabelle Mansuy)和她的同事在小鼠出生后的头两个星期,把它们从自己母亲身边带走并隔离。其中的雄性小鼠长大以后会表现出抑郁症的特点。当把这些雄鼠与正常的雌鼠配对,生出来的下一代显现出与成年鼠相似的抑郁行为,尽管在它们的成长过程中并没有遭受压力。这种压力易感性的传递,与精子和大脑中几个特定基因的DNA甲基化程度相关。

我们实验室做了一个类似的研究。通过社交挫败模式,我们使雄性小鼠陷于长期精神压力之中。然后再等一个月,让这些雄性小鼠交配,我们发现它们的后代对压力明显更为敏感。
接下来,我们让这个实验更进一步。假如使小鼠对压力变敏感的表观遗传修饰真的可以遗传的话,那么这些改变应该会延伸到动物的生殖细胞中。因此,我们从遭受社交挫败的雄性小鼠中取出精子,然后用这个精子使正常母鼠的卵细胞受精。我们发现,这种人为结合所产生的后代几乎完全正常:它们只表现出一点点的焦虑和冷淡的迹象。
这个实验结果并不绝对,因为表观遗传标记有可能在体外受精过程中,由于未知的原因从精子里消失了。然而,这个结果提示,那些和受胁迫的雄性发生自然交配的雌性,与和正常雄性交配的雌性或者那些从来就没见过孩子父亲的雌性相比,它们对待幼崽的方式是不同的。因此,后代的抑郁可能源于一个早期的行为体验,而不是直接通过精子或卵细胞中携带的表观遗传修饰遗传。
这并不是说表观遗传修饰借由生殖细胞进行传递是不可能的。只是我们目前没有可靠的证据来证明它的存在。为了解决这个问题,我们必须开发出实验工具和手段,能够让我们在生殖细胞中发现相关的表观遗传修饰,然后确认这些修饰对于所观察到的行为特征的传递是必要和充分的。
18世纪的生物学家让-巴蒂斯特·拉马克(Jean-Baptiste Lamarck)以其提出的获得性特征的遗传理论而著称。根据这个理论,生物体在后天获得的特性,比如通过锻炼得到的强健的肌肉,可以遗传给他的下一代。
当然,我们现在已经知道,生物个体的基因在决定其生理特征和功能中起统治作用。科学家们也逐渐开始意识到,贯穿于发育和成长期的与外界环境的接触,及不同的经历体验(包括偶发事件)可以改变我们基因的活性,个人行为特征也正是通过这种方式得以体现。并且我们现在明白,表观遗传机制介导了本能和后天教育之间的相互影响。
接下来,我们仍然有很多工作要做,以更全面地了解表观遗传是如何以及多大程度上影响了我们的行为特征、对精神疾病的易感性,以及这类弱点是否会遗传给后代。毫无疑问,拉马克和他的批判者们将会非常愿意一起来探讨这种可能性。
请 登录 发表评论