在名作《我自己的歌》(Song of Myself)中,美国著名诗人惠特曼这样写道:“我包孕芸芸众生”(I contain multitudes)。虽然他并非从生物学角度来思考这个问题,但这句话确实描述了一种生物学现象。近来的研究表明,除了数以亿计由受精卵发育而成的细胞外,我们体内还有来自他人的、遗传性质不同的细胞。当我们还在子宫内时,就从母亲那里获得了这些细胞,而怀孕的妈妈们,体内也有胎儿的细胞。
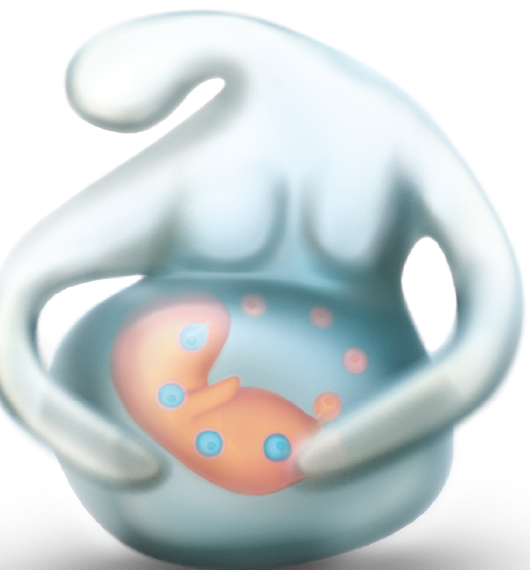
细胞可以穿越胎盘,这并不奇怪,因为连接母亲和胎儿的组织并非不可穿越的屏障,而是像一个交叉地带,选择性地让一些物质通过(比如胎儿生长发育所需的营养物质)。奇怪的是,穿过胎盘的细胞竟可在新宿主体内长期存在,还会在血液中循环,甚至定居在不同的组织——一个人的细胞安全地存在于他人体内的现象,叫微嵌合(microchimerism)。这种现象已经引起科学家的强烈兴趣,因为最新研究显示,它既能促进健康,也可能引发疾病。更好地认识这些“移民”细胞的作用,有助于临床医生去弊存利:利用它们保护人类健康,避免可能出现的破坏作用。
细胞移民
60多年前,一篇公开发表的论文称,母亲的皮肤癌细胞可以进入胎盘和胎儿体内。在这篇论文的启发下,科学家进一步研究发现,其他母体细胞也可以进入胎盘和胎儿体内。上世纪60年代,又一个发现震惊了生物学家们:母体内正常的血细胞也能通过胎盘进入胎儿体内。
研究资料显示,细胞还可以反向移动:从胎儿进入母体。最早发现该现象的时间,可以追溯到1893年。当时,在一名死于妊娠高血压病的妇女的肺脏中,一位德国病理学家发现了来自胎儿的细胞。但此后近百年时间里,关于健康母亲获得胎儿细胞的报道非常少。直到1979年,一篇里程碑式的论文引起了科学界的注意:美国斯坦福大学医学院的莱纳德·A·赫岑伯格(Leonard A. Herzenberg)及其同事在一篇论文中称,他们在一名怀有男性胎儿的妇女的血液中,发现了男性细胞(含有Y染色体)。
不过,真正让生物学家感到的惊讶的,并非母亲和胎儿细胞可以双向“流动”,而是少数“移民”细胞可在健康个体内长期存活。上世纪90年代,生物学家在研究细胞从母亲向胎儿转移的现象时发现,母体细胞可以长期存活在患有重症联合免疫缺陷(severe combined immunodeficiency,患者体内缺乏抗感染的关键免疫细胞)的儿童体内。生物学家最初的看法是,这类儿童体内存在微嵌合现象的原因,是因为他们缺乏免疫应答功能。一般说来,正常的免疫系统会摧毁潜藏在儿童体内的母体细胞。
事实却否定了这个被广泛认可的观点。我和同事发现,即便免疫系统功能正常,成年人体内也有母亲的细胞——我们的研究对象甚至包括一位46岁的中年人。而早在几年前,美国塔夫斯大学的黛安娜·W·比安基(Diana W. Bianchi)就已经发现,胎儿细胞同样能在母体内长期存在。她在一位儿子已长大成人的中老年妇女体内,检测出了男性的DNA(在很多研究中,研究人员估算妇女体内男性细胞数量的方法,主要是测定妇女血液或组织标本中男性DNA的量,即Y染色体)。
为什么“移民”细胞可以存活这么久?大多数细胞都受到寿命限制,存活一段时间后就会死亡。只有干细胞例外,可以无限分裂,分化成各种特定细胞(比如免疫细胞或其他器官中的细胞)。长期存在的微嵌合状态意味着,第一批外来细胞可能是干细胞或类似干细胞的细胞。随后的研究证实了这种假设。我有时在想,这些转移到他人体内的干细胞就像种子,它们分布在全身各处,在那里扎根,变成身体的一部分。
“双刃剑”
在后代体内,母体细胞就像一把双刃剑(母亲的细胞存在于后代体内,叫做母源微嵌合态,maternal microchimerism)。首先,母亲的细胞可能引发自身免疫疾病,让免疫系统攻击自身组织。青少年皮肌炎(dermatomyositis)就是一种自身免疫疾病,受损部位主要为皮肤和肌肉,母体细胞在发病过程中似乎起着推动作用。2004年,美国梅奥医学中心(Mayo clinic)的安·M·里德(Ann M. Reed)的研究表明,从病人血液中分离出来的母体免疫细胞,会与病人的其他细胞发生反应。因此,里德和她的同事认为,引发青少年皮肌炎的祸首,很可能就是孩子体内的母体免疫细胞。
新生儿狼疮综合征(neonatal lupus syndrome)似乎也与母源微嵌合态有关。科学家曾认为,具有杀伤活性的抗体,从母体血液循环进入发育中的胎儿体内,是引发该病的原因之一。这些抗体会与胎儿的组织细胞结合,让新生儿面临各种疾病的侵袭,最严重时可能引发致命的心脏炎症。
然而,血液循环中本身就有杀伤性抗体的母亲们却是健康的,她们生下的孩子通常也很健康。我和同事根据该现象推测,在新生儿狼疮综合征中,抗体或许是病因之一,但肯定还有其他因素在起作用。在检查死于心脏衰竭的新生儿狼疮患者的心脏组织时,我们研究小组的安妮·M·史蒂文斯(Anne M. Stevens)发现了患者母亲的细胞,而在死于其他疾病的胎儿尸体中,这种现象极为罕见。史蒂文斯还发现,患者体内80%以上的母体细胞都能产生蛋白质,这说明它们不是循环中的血细胞,而是心肌的组成部分。(译者注:近来研究证明,造血干细胞可以分化为心肌细胞)。

2003年,史蒂文斯发表了关于上述发现的研究报告,这让很多科学家意识到,在新生儿狼疮中,患者免疫系统的攻击目标很可能是母体来源的心肌细胞。这也间接证明,从母体转移到胎儿的细胞,应该是干细胞或类似干细胞的细胞,因为患儿体内的母体细胞已经分化成心肌细胞,并整合到患儿的心脏组织中了。或许,一些“自身”免疫疾病的发病过程,就是患者的免疫系统恶性攻击某个组织中的移民细胞。对于不含移民细胞的组织,免疫系统不会发起免疫攻击。
但其他研究显示,母体干细胞的分化与整合有时并不会引起免疫攻击,反而有利于受损器官的修复。Ⅰ型糖尿病(胰岛素依赖型)多见于儿童和年轻人,患者胰腺中分泌胰岛素的β细胞会被免疫系统破坏。2002年,在研究母源微嵌合态与Ⅰ型糖尿病(胰岛素依赖型)间的关系时,我们推测,在妊娠期间,母体细胞会进入胎儿胰腺,并在那里“定居”,分化成β细胞,最后成为免疫攻击的目标。
推测只对了一半。与正常人相比,在Ⅰ型糖尿病患者的血液中,母源微嵌合现象更普遍,嵌合程度也更高。病理解剖时,我们在糖尿病人的胰腺中,找到了来源于母体、能产生胰岛素的细胞。但令人吃惊的是,在非糖尿病人的胰腺内,我们也发现了这样的细胞,而且没有任何证据可以证明,这些细胞就是免疫系统的攻击目标。相反,我们的研究结果却证实,糖尿病患者胰腺内的母体细胞有恢复胰腺功能的作用。这就说明,如果能找到一种方法,诱导母体细胞增殖、分化,以修复受损组织,就可以将微嵌合体现象转变为有效的治疗方法。
胎儿细胞带来的麻烦
与母源微嵌合体一样,胎儿微嵌合体(fetal microchimerism,即母体内存在有胎儿的细胞)也具有两面性。我首先发现的是胎儿微嵌合体可能带来的害处。在知道健康人体内长期存在母源微嵌合现象之前,杰夫·霍尔(Jeff Hall)的发现已让我感到非常震惊。霍尔当时在美国西雅图CellPro生物技术公司工作,主要负责孕妇的产前诊断。1994年的一个晚上,我从电话中得知,霍尔实验室的一位女技术员生下儿子一年后,血液中竟然还有胎儿细胞。于是我开始思考,孩子的细胞长期存在于母体内会导致什么后果?母亲自身的细胞与胎儿细胞间的相互作用,是否会导致自身免疫疾病?
这个新想法让我兴奋起来。1996年,在一篇公开发表的假说性论文中,我把在不同医学领域观察到的现象汇集在一起,对自身免疫疾病的传统看法提出了质疑。
首先,这类疾病在女性中的发病率高于男性,40~60岁的妇女是高危人群。在该年龄段的妇女中,多次怀孕的人并不少见,因此,将发病原因归咎于激素水平的周期性变化是不确切的(译者注:一般说来,这个年龄的妇女已经停经)。如果致病祸首是长期存在的胎儿细胞,我们可以推测,在已生过孩子的妇女中,自身免疫疾病的发病率是最高的。
第二个想法来自移植领域。在实施移植手术之前,医生必须找到与病人遗传特性相匹配的移植器官,确保器官提供者与接受者的人白细胞抗原(human leukocyte antigen,简成HLA,一种细胞表面分子)相似或一致。如果供者与受者的HLA明显不同,受者的免疫系统将会排斥移植器官,并摧毁它,从而引发疾病。反过来,如果供者的细胞不甘心被消灭,竭力生存,移植器官就可能引发移植物抗宿主病(graft-versus-host disease)。在这种情况下,供者器官中的免疫细胞就会攻击受者的组织,导致受者皮肤发硬、肠道内皮细胞受损,甚至肺脏被破坏。
移植物抗宿主病的症状与一类自身免疫疾病——硬皮病很相似。这种相似性意味着,母体内的胎儿细胞可能与硬皮病的发生有关。我向比安基提议,两个实验室合作研究这个问题。在人体内,细胞数量之多超乎想象,要鉴定某一种细胞无异于大海捞针。不过,由于只有男性细胞才具有Y染色体,在妇女体内寻找男性细胞相对容易,因此我们决定以生过男孩的妇女为主要研究对象:从患有硬皮病和健康母亲身上采集血样和组织标本,从中寻找含有Y染色体的细胞。
研究中,首次在硬皮病患者身上观察微嵌合体现象时,我们就发现,患者体内的胎儿细胞的确与疾病相关——在病人血液中,微嵌合程度要比健康妇女高。在另一项研究中,我们和美国托马斯·杰弗逊大学的塞尔吉奥·A·希门尼斯(Sergio A. Jimenez)分别发现,在患者的皮肤和其他病变组织中,也存在胎儿微嵌合现象。
但引起我们兴趣的是另一种现象。HLAⅡ也是一类HLA分子,在患有硬皮病的妇女体内,胎儿细胞表面的HLAⅡ类分子与母体细胞很相似,而在正常妇女体内,这种相似性要低一些。我们猜测,妇女患硬皮病的主要原因是,胎儿细胞与母体细胞的HLA过于相似,很容易逃过母体免疫系统的追杀。而在正常情况下,胎儿的基因一半来自母亲,一半来自父亲,HLA的基因也是如此,因此胎儿细胞的HLA与母体细胞应该有50%的差异——如此大的差异很容易被免疫系统识别、清除。
未被免疫系统清除的胎儿细胞将会以多种方式给母体带来麻烦。如果在某种外界因素的作用下,母体免疫系统“意外”获得了识别胎儿细胞的能力,并试图清除这些细胞时,就可能引发自身免疫疾病,因为胎儿细胞与母体细胞太相似,免疫系统很可能误伤自身组织。胎儿细胞也可能已成为母体免疫系统的成员,干扰免疫系统的鉴别能力。
微嵌合是一个非常新的研究领域,还有不少问题需要进一步研究才能解决:母亲从怀孕开始,胎儿细胞就与母体免疫系统“和睦相处”,为什么在几十年后,它们突然会受到免疫系统的攻击?怀孕后,母体免疫系统对胎儿细胞的耐受性是如何形成的?
怀孕改善病情?
在什么情况下,胎儿微嵌合态能为母体带来好处?理论上,在母体免疫系统功能低下时,母体内的胎儿免疫细胞会对致病微生物产生强烈的免疫反应。在这种情况下,胎儿细胞就是母体免疫系统的帮手。它们也可能修补一些受损组织。尽管胎儿细胞可能引起某些自身免疫疾病,但我们有一些间接证据表明,它们实际上有助于改善某些自身免疫疾病的病情,比如类风湿性关节炎(rheumatoid arthritis)。这种疾病的特点是持续时间长、关节肿痛。
70年前,美国科学家菲利普·S·亨奇(Philip S. Hench, 1950年诺贝尔生理学或医学奖得主)发现,在妇女怀孕阶段,类风湿性关节炎的症状会得到缓解,有时甚至会消失,但分娩几个月后又会复发。最初,医生们把这一现象归咎于激素(特别是皮质激素)的变化,认为这是激素水平增高2~3倍的结果。但激素水平不能完全解释这个现象,因为一些孕妇体内的激素水平偏低,类风湿性关节炎症状也会得到缓解,而有些孕妇体内的激素水平偏高,关节炎却一如既往地困扰着她们。
由于怀孕会刺激免疫系统(在遗传上,胎儿与母亲仅有50%的相似性),我们联想到,类风湿性关节炎的病情反复或许与免疫反应有关。1993年,我们在某些孕妇身上观察到,当胎儿与母体的HLAⅡ分子差异很大时,类风湿关节炎的症状就会得到改善。这似乎是一种暗示:母亲与孩子间HLAⅡ分子的差异,可能就是关节炎病情反复的原因。后来,我们又发现孕妇体内胎儿微嵌合的水平越高,类风湿性关节炎症状的缓解程度也越明显;同样,微嵌合程度骤然下降,则会导致产后类风湿性关节炎突然发作。不过,我们还不知道为什么胎儿微嵌合态程度越高,或HLAⅡ分子差异越大,孕妇的类风湿性关节炎症状的改善也越明显。
迄今为止,研究人员已针对身患不同疾病的母亲们,检查了多种器官中的胎儿微嵌合态,如甲状腺、肠道、肝脏等。有些胎儿细胞已经定居在母亲的器官内,有些则表现出了这种倾向。在母亲们的免疫系统中,胎儿微嵌合现象也已得到证实。胎儿微嵌合到底有害还是有益,可能对不同的人会有不同的影响。
未解谜团
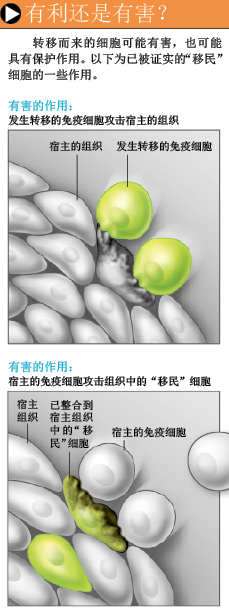
总的来讲,微嵌合能以某些方式影响健康。发生转移的免疫细胞可能攻击身体组织,引发自身免疫疾病(如青少年皮肌炎);也可能适应母体环境,分化成身体的组织,成为宿主免疫系统攻击的目标,硬皮病和新生儿狼疮就是这种情况;还有一种可能是,这些细胞能缓解疾病,帮助受损组织再生和功能修复,正如在Ⅰ型糖尿病看到的那样。
上述每个现象都可能催生一种新疗法。如果嵌合细胞是攻击者,我们可以设法选择性地将它们去除,或抑制它们的活性;如果它们成为母体免疫系统的攻击目标,可以诱导免疫系统对它们产生耐受性;如果它们可以帮助受损组织再生,可以设法刺激它们,以缓解因组织破坏引起的疾病。
尽管只有在妇女身上,才会出现胎儿微嵌合现象,但母体细胞却可出现在男人、儿童以及从未怀过孕的女性身上。由于母源微嵌合态早在胎儿发育过程中就建立了(此时免疫系统也正在发育中),而胎儿微嵌合态是在免疫系统已经成熟的母体内建立的,因此上述两种过程中,转移方向相反细胞的经历有很大的差别——正如一个人移民到正在形成和已经形成的国家,他的经历也是不同的。但我们对这种差异的理解还不够深入,另一个很有趣的问题也尚未解决:在妇女体内,既有来自母亲的细胞,又有来自自己一个或多个孩子的细胞,这两类或几类细胞会对健康产生怎样的影响?
微嵌合现象是生物学领域的一个新课题,它动摇了免疫学中关于“自身”的传统定义。在每个人的生命之初,微嵌合态可能就已经与我们如影随形,因此我们和其他科学家的发现支持这样一种观点:“自身”不仅包括从受精卵发育而来的细胞,还有天然获得的细胞。最近一项研究发现,小鼠的大脑也会出现母源和胎儿微嵌合态。这一发现引发了一系列问题:母体细胞会影响小鼠大脑发育吗?是否可以“驯化”胎儿细胞,用于治疗神经退化性疾病?如果我们的大脑并非完全由自己的细胞组成,那么是什么建构了“心理自身”?
请 登录 发表评论