阵阵抽痛、奇痛难耐、疼痛不安、剧痛难忍、痛心切骨、痛入心脾、痛不欲生……
疼痛实在让人痛苦。无论是排泄肾结石时烧灼般的剧痛,还是虎钳般紧紧挤压的偏头痛,所有的疼痛都有一个共同之处:忍受疼痛的人都希望疼痛能消失得无影无踪。
但目前广泛使用的镇痛药,基本上都是已有数百年历史的民间偏方:由罂粟制成的吗啡和鸦片、由柳皮制成的阿司匹林。尽管在一定程度上,这些药物都能缓解疼痛,但是每一种药物又有局限性。阿司匹林和其他一些非甾体类消炎药物(NSAIDs),例如布洛芬,只对一般性疼痛有效,却无法缓解剧痛。就算是“镇痛之王”——鸦片,也无法让所有人免受疼痛之苦。此外,这几类药物还有两大致命的缺陷:它们有严重的副作用,病人会对它们产生耐受性,需要逐步提高剂量方能缓解疼痛。
在过去二十年间,神经生物学家对承载痛感信号的特殊分子和细胞通路已有了全面的认识。今天,在这些认识的指引下,人们正在设计新型镇痛方案:有效镇痛,无副作用。事实上,还有许多镇痛方案处于研究阶段,本文略举其中一二。
疼痛为何物
17世纪,法国哲学家勒内·笛卡尔(Rene Descartes)提出了一种理论,对疼痛的产生过程作出了阐释。在他看来,捏拧挤压、劈砍重击或戳捅刺插,这些行为实质上都是在猛拽神经索,然后这根神经索拉响大脑中的警铃。比如一只脚被烧伤了,我们立即感到疼痛。对此,笛卡尔这样解释:“快速运动的火粒子”会产生一种骚动,“沿着神经纤维,直抵大脑”。
笛卡尔的理论并非不着边际。疼痛通常起始于外周神经系统:皮肤里的某个内部器官或中枢神经系统(CNS,包括大脑和脊髓)以外的任何部位。当脚趾碰到或靠着滚烫的火炉时,便会激活一类神经细胞:疼痛感受器。在两种情况下,疼痛感受器会作出反应:一是遇到伤害性刺激,例如极端温度(烫或冷)、机械压力;二是遭遇在受伤或发炎时所产生的化学物质。
疼痛感受器有两个分支,其中一个相当于感觉检测器,向外伸出,到达外周神经系统,在此可以支配组织的活动;另一个分支则向内伸入,进驻脊髓。感受器的细胞体位于脊髓外的一个结构中,处在两个分支之间。当外周分支上的特定检测分子遇到皮肤或某一器官里的有害物质时,它们就会触发一个脉冲,上传到该分支线路,沿着中枢分支,到达后角(脊髓的一个区域)。在后角区,疼痛感受器释放神经递质(一种信号分子),激活后角区的神经元,促使神经元将警告信息上传给大脑。虽然疼痛感受器经常被称为痛感神经元,但是它们的功能仅仅是发现潜在的有害刺激物,并向大脑发出信号。大脑才是将信号转换为疼痛,并促使我们失声喊出“哎哟”的器官。
疼痛不是只有负面作用,它也有“善良”的时候。例如,当我们扭伤或擦伤之后,尖锐的疼痛随之而来。这不是为了让我们难受,而是为了保护我们:提醒我们小心,避免伤情加重。这种疼痛往往是暂时的,随着时间的推移会逐渐消失。
最让病人和医生烦心的,是那种不会消失、难以缓解的疼痛。很多时候,当受伤或炎症久治不愈,恼人的疼痛就会缠着我们不放。关节炎的疼痛源于持续不断的炎症反应,而让癌症患者生不如死的剧痛,则是由大范围的组织受损和发炎所致。
另外,有些持久不去的疼痛属于神经性疼痛,源于神经细胞自身受损。当CNS中的神经元持续受到多发性硬化(例如中风或脊髓受伤)损伤时,疼痛还会加剧。神经痛也可能源于末梢神经元受到的损伤。尽管伤腿已被截去,但伤腿上的疼痛仍让截肢患者痛苦不堪(幻肢疼痛);尽管疱疹已经消退数年,但疱疹患者的皮肤仍有烧灼感(疱疹后神经痛),这些都是神经痛的典型症状。这种症状难以消停,并非是持续性损伤或其他疾病的征兆,而是因为神经痛本身是一种神经系统疾病,需要疼痛专科医生才能对付它。
无休止的疼痛
有一种疼痛难以医治、难以控制,被它缠住的人都有一个共同特征,那就是对外源刺激异常敏感。这种敏感性有两种表现形式:痛觉过敏(对一般痛感输入信号的一种过度反应)和异样疼痛(非疼痛刺激也能引起疼痛感觉)。对于一般人,穿衣服、弯关节,是再正常不过的行为,但是对异样疼痛患者而言,却可能带给他们无法忍受的痛苦。
目前,生物学家认为,这类高敏感性(敏感化)的根源,可能是神经细胞的分子或结构发生了变化。例如,在外周神经系统,引发炎症的分子可能让疼痛感受器对输入信号作出过度反应。甚至在不存在任何输入信号的情况下,炎症分子也能使疼痛感受器产生痛感信号。
CNS发生改变,痛感传导途径过度活跃,也可能导致敏感化。CNS的改变不仅持续时间长,而且形式多样。包括受体数量的增加(这是对疼痛感受器释放的神经递质作出响应),神经元连接通道的重配,以及抑制痛感信号发出的神经元的丧失。当CNS本身也被牵连其中时,敏感化前面就得加一个定语,称为中枢敏感化。
事实证明,任何步骤都不能有半点差池,否则持续的疼痛就会导致敏感化,使不适感加重、时间延长。因此,在寻找新的镇痛方法时,许多研究人员把改善痛觉过敏和异样疼痛视为首要问题。与此同时,病人必须认识到,他们不应一味忍受无休止的疼痛,积极治疗、防止敏感化加剧,才是万全之策。
抑制环加氧酶
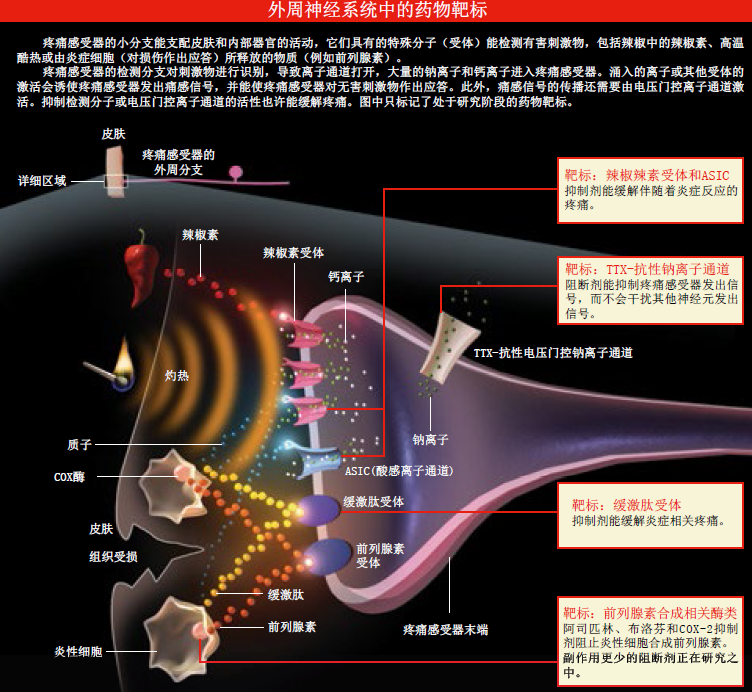
在研究新的镇痛方法时,研究重点大多集中于神经末梢——伤痛信号的发源地。某些疼痛感受器用于检测有害刺激物的特殊分子,极少在人体的其他部位出现。由此可以推测,限制这些分子的活动,就可以关闭痛感信号,并且不会影响其他生理过程,也不会引发副作用。
目前使用最广泛的镇痛药物——阿司匹林和其他NSAIDs,主要在外周神经系统行使职责。当某个组织受伤时,这一部位的各种细胞就会分泌一种化学物质——前列腺素,作用于疼痛感受器的痛感分支,降低该分支的活化阈,从而提高伤者对疼痛的敏感性。阿司匹林和NSAIDs正是通过提高痛感分支的活化阈,来达到镇痛的目的:抑制环加氧酶(前列腺素合成过程中的关键酶)的活性,阻止细胞合成引发疼痛的前列腺素。这些非处方药可以缓解日常疼痛,但是它们还会抑制人体其他部位的前列腺素合成,常导致胃痛、腹泻和溃疡之类的副作用。因此,这些药物不能长期使用,用药剂量也必须严格控制。
为了减少对胃肠道的伤害,一些制药公司正在开发一类以环加氧酶-2(COX-2)为靶标的药物。由于COX-2通常并不在胃肠道中起作用,因此抑制它的活性不会像传统NSAIDs那样对胃肠道造成伤害。但是,这些药物的实际效果还有待检验。同时,这些药物自身也存在问题。Rofecoxib(Vioxx)是一种COX-2抑制剂。作为处方药,它被用于缓解关节炎疼痛。但人们却发现,它会增加心脏病发作和中风的危险。于是,Rofecoxib被判死刑。对于其他COX–2抑制剂是否有副作用,还在调查之中。
辣椒素受体
研究发现,有些靶标几乎仅存在于疼痛感受器中。针对这些靶标,可以开发一些具有选择性的药物,只作用于某种或某些靶标。这样不仅可以缓解疼痛,而且无副作用。最引人注目的靶标,当数辣椒素受体。该受体存在于许多疼痛感受器的膜中,是一种离子通道,主要对辣椒素(辣椒粉中的刺激性成分)、高温和质子(使物质变为酸性的氢离子)作出应答。当我们身体的某个部位发炎(在发炎的组织中,质子的含量异常丰富)、所处环境的温度超过43℃、或正在享用辛辣食物时,离子通道(辣椒素受体)就会打开,让大量的钠离子和钙离子涌入疼痛感受器,促使它产生一种信号,然后把信号转化为灼热感。
因此,抑制辣椒素受体的药物可使炎症疼痛得以减轻。动物试验发现,尽管肿瘤已转移到骨组织,并损伤了骨组织,但辣椒素受体拮抗剂仍能缓解由肿瘤周围的酸性环境引起的剧烈疼痛。目前,多家制药公司正在争先恐后地研发辣椒素受体拮抗剂。
好戏还在后面。令人啼笑皆非的是,有时故意刺激辣椒素受体竟然也能减轻疼痛!HIV感染、疱疹和糖尿病的发作会引起神经损伤,往往伴随着刺痛和灼痛;手术后,逐渐愈合的伤口会奇痒无比。这时,含辣椒素的外用乳膏就派上用场了,它能缓解搔痒和疼痛,让病人不再坐立不安。尽管辣椒素缓解疼痛的确切机理还不清楚,但很可能是由于随着时间的推移,小剂量的辣椒素降低了受体对外源刺激的敏感性;还有一个原因,可能是疼痛感受器释放的神经递质被消耗殆尽。
阻断离子通道
在疼痛感受器的外周分支末端,发现了一类与众不同的分子——钠离子通道。作为一种药物靶标,它越来越引人关注。所有的神经元都具有钠离子通道,神经元细胞膜内外两侧的电压变化,决定着钠离子通道的开关。电压的变化会产生脉冲,将信息从一个神经元传递到另一个神经元。局部麻醉可以暂时钝化钠离子通道,目前它被用于消除各种类型的疼痛——从跌打损伤到牙科手术。但局部麻醉只能应用于患处,假如整个神经系统的钠离子通道都被钝化,将足以致人于死地!
不过,希望并没有完全破灭:痛感神经元拥有电压门控钠离子通道的一个亚群——TTX-抗性离子通道,而CNS中没有这种离子通道。因此,能阻断TTX-抗性离子通道的药物便可用于系统性(全身)治疗,而无副作用。还有研究指出,这类药物可以抑制受伤外周神经的过度活性,因而能缓解神经痛。遗憾的是,制药行业至今都未能成功研制出针对TTX-抗性离子通道的选择性抑制剂。部分原因在于,这类通道酷似TTX-敏感性钠离子通道,而后者广泛分布于整个神经系统。
也许,一种新兴技术——RNA干扰,能选择性地抑制TTX-抗性离子通道。RNA干扰技术的关键在于,要将一些小分子——小干扰RNA(siRNA)引入生物体中。siRNA进入生物体后,就会引起mRNA(指导蛋白质合成的分子)的降解,从而阻止相关蛋白的合成。尽管这一技术正在某些视网膜病患者中进行试验性研究,但是利用RNA干扰技术来消除疼痛,仍然极具挑战性。和基因疗法一样,RNA干扰的方法很可能需要用一种病毒来传送siRNA,而病毒又牵涉到安全性问题。这种方法是否切实可行,还有待证明,但它还是让人激动不已。
近年来,制药公司还在研发一种号称“魔术弹”的镇痛剂:它能专一、高效地抑制痛感传导分子的活性。这种镇痛剂是否真能让病人摆脱难缠的疼痛?答案可能会让很多人失望,因为仅仅关闭痛感传导途径的一个信号入口,还不足以完全镇痛。
例如,当外周组织出现炎症反应时,就会产生一种小分子蛋白质(肽):缓激肽,它能强有力地刺激疼痛感受器。只要抑制缓激肽受体,就能阻止它们激活疼痛感受器。但是,组织受伤或发炎还会产生质子和前列腺素,而抑制缓激肽受体的拮抗剂并不能阻止神经元识别质子和前列腺素,更无法阻止神经元作出应答。那么,抑制了辣椒素受体就能减轻所有质子介导的疼痛吗?答案同样是否定的,因为在某些情况下,质子还会激活疼痛感受器上的酸感离子通道(ASICs),这是一种单一类别的检测器。
聚焦脊髓
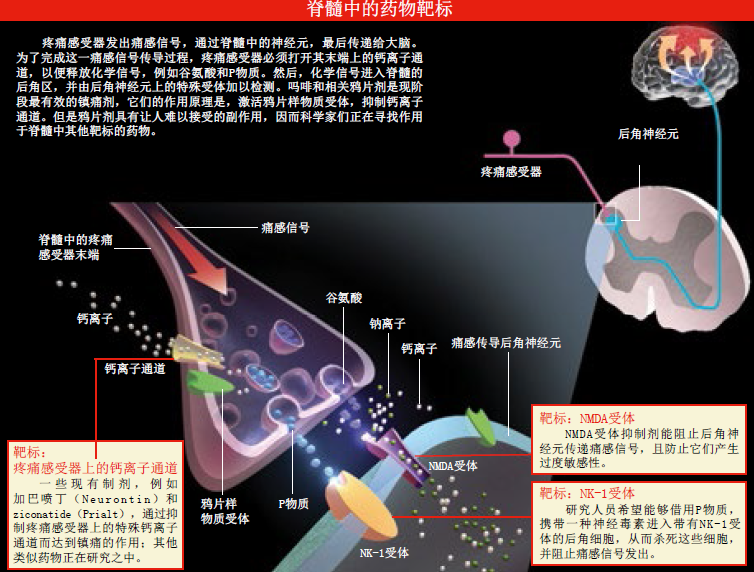
疼痛的生理机制错综复杂,科学家们提出了两种解决方案:一是鸡尾酒法,即针对各种疼痛机制,将抑制剂药物调和在一起,同时用药;二是终端法,即以CNS内的一些重要分子为药物靶标,阻止所有疼痛感受器发出的痛感信号传送至脊髓——不论刺激源为何物。
吗啡以及其他鸦片剂采用的正是第二种策略:与伸进脊髓中的疼痛感受器末端上的鸦片样物质受体结合。通过激活受体,鸦片剂会抑制神经递质的释放,从而阻止痛感信号传送到脊髓神经元。此外,鸦片剂还能使后角神经元对痛感信号的应答变得迟缓。由于鸦片剂在脊髓中发挥药效,因此在理论上,它们能缓解所有类型的疼痛,虽然最适合它们干的工作是消除炎症疼痛。
然而,带有鸦片样物质受体的神经元遍布全身,包括大脑和胃肠道系统中的神经元。因此,吗啡及类似药品会带来一大堆副作用,包括严重便秘与呼吸中断。为了保证安全,病人用药或者医生开处方时,必须限制药物剂量。此外,鸦片剂容易让病人上瘾,因而医生不愿意开具鸦片剂的处方——尽管因使用鸦片剂镇痛而上瘾的病人并不常见。为了减少副作用,鸦片剂常被直接输入脊髓周围充满液体的空隙中(鞘内)。注射(用于手术后疼痛)或借助于留置泵(用于慢性疼痛)也是常用给药途径。
鸦片剂的替代药物同样具备缓解疼痛的能力。干扰钙离子通道的药物,能阻止脊髓中的疼痛感受器末端释放神经递质。加巴喷丁(Gabapentin,即Neurontin)是一种抗惊厥药,通过与某些钙离子通道的一种特异亚基相互作用,它能缓解某些形式的疼痛。ziconatide(Prialt)是一种相对较新的药物,源于一种太平洋锥形蜗牛的毒液。它可以抑制另一类钙离子通道:N型钙离子通道。
与鸦片样物质受体一样,N型钙离子通道遍布整个神经系统。如果ziconatide在全身传送,那么血压可能会猛然下降,因此这种药物只能在鞘内供给。虽然能镇痛,但在CNS内,ziconatide仍会产生令人不适的副作用,包括头晕、恶心、头痛和意识模糊。因此,ziconatide的服用者,基本上都是那些别无他法的晚期癌症患者〔参见《科学美国人》2005年4月号加里·斯蒂克斯所著《一种镇痛的毒素》一文〕。
镇痛研究有了新进展。最近,一种以大麻素受体(传递大麻效力的受体)为靶标的药物,正在通过临床试验稳步前进。这类药物似乎能以多种方式缓解疼痛:干扰疼痛感受器与其靶细胞之间的信号传递;让蠢蠢欲动的炎症细胞变得安分。
关闭疼痛之门
阻断痛感信号向脊髓传送可以缓解疼痛,那么阻止脊髓神经元对痛感信号作出应答,是否可以达到同样的效果呢?研究人员正在努力寻找答案。疼痛感受器释放的神经递质,特别是谷氨酸,是痛感信号的主要载体。谷氨酸会激活脊髓后角区中的各种受体。其中,NMDA(N-甲基-D-天冬氨酸)类谷氨酸受体与中枢敏感化有关。因此,在理论上,这类受体是新型镇痛剂的作用靶标。
各种类型的NMDA受体存在于体内的每一个神经元。因此,假如所有类型的NMDA受体都被抑制,那么可能会引起灾难性的后果,包括失忆、抽搐以及瘫痪。为了避免悲剧发生,研究人员将目标瞄准了只有后角区才有的、含有NR2B亚基的NMDA受体。在动物试验中,能与NR2B亚基相结合的药物表现非常出色,让人振奋。例如,将一种NR2B抑制剂直接输入小鼠的脊髓,然后观察小鼠对疼痛的敏感性。结果显示,较之未接受抑制剂的小鼠,这些小鼠对疼痛的敏感性的确下降不少。另外,这种药物对异样疼痛也很有效,能让外周神经受伤的小鼠免受痛苦。
很多疼痛感受器还释放肽类神经递质,如P物质和降钙素基因相关肽(CGRP)。通过作用于分散的受体,这些肽会激活脊髓中的痛感传导神经元,因此,阻断肽与受体的相互作用就有可能缓解疼痛。可惜事与愿违,选择性的阻断P物质的受体(神经激肽-1受体,简称NK-1受体)未能有效缓解疼痛,临床试验宣告失败。也许,仅仅阻断NK-1受体还远远不够。抑制CGRP在脊髓中的活性能否镇痛?虽然答案已变得扑朔迷离,但制药行业仍在研发拮抗剂,旨在干扰CGRP释放到大脑表面的血管上,以缓解剧烈的偏头痛。
杀死痛感信使
如果方法用尽,仍无法阻止痛感信号传送至神经中枢,那么就只能对相关神经痛下杀手了。但正如前面所提到的,神经损伤产生的疼痛更为顽固、更为持久,因此切断痛感神经后,病人往往会更痛苦。脊髓前侧柱切断术(即切断脊髓中向大脑传递痛感信号的途径)曾普及一时。但近年来,该方法只能用于垂死的癌症晚期患者,其缺陷在于,外科医生不能选择性地切断痛感传导途径。
正当大家苦寻对策之时,一种神奇的分子疗法出现了,并在动物实验中大获全胜。于是,人们纷纷将目光投向它。这种方法的关键,在于选择性地除去一类脊髓神经元(这类神经元接收来自疼痛感受器的输入信号)。如何才能作出“选择”呢?一种毒素(皂草素)与P物质的连接便是“选择”的开始:先把皂草素与P物质连接在一起,再让P物质与NK-1受体相结合,接着,整个连接物便进入神经元,然后,连接物释放皂草素,杀死神经元。因为连接物只能进入具有NK-1受体的细胞,所以研究人员希望借此减少副作用。
但是,除非万不得已,否则不能随便杀死脊髓中的神经元:CNS中的神经元不会再生,杀死神经元所引起的改变,无论是好是坏,都将是永恒的。而外周神经系统中的神经纤维可以再生,切断它们不会引起永久性改变。因此,从理论上来说,削减疼痛感受器的信号检测分支的方法优点多多:不仅可以镇痛,而且受损分支最终还能再生,失去痛感检测能力的组织还能恢复正常。
将神经元作为靶标,可能并非征服疼痛的唯一方式。研究表明,神经胶质细胞(具有分裂能力,可增生为神经元)与疼痛有关,它会对外周神经的损伤作出应答。神经胶质细胞首先会迁移到与受伤神经有关的后角区域。然后,排放出一组化学物质,促使脊髓中的疼痛感受器末端释放神经递质,维持痛感信号。上述化学物质中的一些成分,如生长因子和细胞因子,也会使后角神经元变得过于兴奋,因而抑制过度兴奋有助于消除过度敏感。当神经元受伤时,一些分子会自动招集并激活神经胶质细胞。目前,多个研究小组正在致力于鉴别这些分子,并想法抑制它们的活性。
有趣的是,前列腺素是活化的神经胶质细胞在脊髓中释放出的关键物质之一。在脊髓中,通过阻断后角神经元上的甘氨酸受体(甘氨酸是一种抑制性神经递质,通常会束缚这些神经元的活动),前列腺素同样能增强痛感。因此,除了干扰外周神经元中前列腺素的产生(常见方式)外,NSAIDS还可以通过抑制神经胶质细胞产生前列腺素(抑制COX酶的活性),以达到镇痛的效果。直接将COX抑制剂输入脊髓,就可以最大程度地减少全身用药带来的副作用。强化甘氨酸受体活性的药品,可能也有助于阻断痛感信号向大脑的传递。
认知疗法
在本文中,我们讨论了一些缓解疼痛的实验性方法。在动物研究中,大多数方法都已露出成功的曙光。有些方法对正常疼痛没有丝毫影响,而对炎症和神经疼痛却有明显效果,并且其副作用也在可接受的范围之内,这怎能不让人激动?但是,这些方法真能帮助病人摆脱疼痛吗?它们对所有的疼痛都有效吗?对于这些问题,目前仍无法给出答案。
一种行为性的非药物疗法值得深入研究,它可以用于治疗顽固性疼痛——特别是与纤维肌痛和应激性(过敏性)肠道综合征有关的疼痛(这类疼痛是否源于器质性病因尚无人知晓)。大约10年前,麦吉尔大学的研究人员证明,催眠能影响大脑活动以及人们对疼痛的知觉。科学家对自愿者进行催眠,并暗示他们的双手浸泡在热水中:热水浴要么舒适,要么痛苦,感觉因人而异。
使用PET扫描监测大脑活动,研究人员发现,在催眠前后,躯体感觉皮质(只对外界刺激作出应答)的活动状态并未改变。但当受试对象认为刺激让自己更不舒适时,其第二脑区(扣带皮质)表现得更为活跃,这表明,催眠改变了个体对疼痛的感知方式。对大脑调节痛感体验的认识多多益善,这将有利于研究人员开发更好的认知疗法,以调节疼痛知觉。
美国女诗人埃米莉·狄金生(Emily Dickinson),经常思索疼痛。在一首诗中,她写道:
疼痛有一种元素叫做空白;
无法记起,
它何时到来,
何时离去。
疼痛没有未来,只有自己。
我们只能希望,对疼痛机理持续不断的研究,能催生安全有效的消除疼痛方法,让疼痛成为永远的过去。
请 登录 发表评论