囊性纤维有望根治
囊性纤维化至今仍是一种无法治愈的“绝症”,会影响全身多种器官,困扰着全球成千上万的人,而且致病基因还会遗传。通过研究这种疾病的基本生物机制,科学家或将找到对付它的有效办法。
撰文 史蒂文·M·罗(Steven M. Rowe) J·P·克兰西(J. P. Clancy)
埃里克·J·索斯切尔(Eric J. Sorscher)
翻译 冯志华
1989年,科学家发现了导致囊性纤维化(cystic fibrosis)的基因缺陷。这是一种严重的遗传性疾病,欧洲儿童是最主要的受累人群。这一发现让很多人看到了希望,似乎期待中的治疗方法很快就能面世——毕竟,很多实验室的研究已经证实,只要导入正确的基因拷贝,就能让病人产生正常蛋白。世界上,成千上万的人正饱受囊性纤维化的折磨,他们中有很多人在20多岁就因病早逝(现在大约有一半的患者能活到30多岁),一旦该疗法得以成功,这些患者或将重获健康。现在的问题是,科学家能否稳妥地将正确基因插入患者的相应组织,进而永久性地根除囊性纤维化。
这项任务的难度超乎所有人的想象。尽管科学家成功构建了一些病毒载体,用于将正确的基因拷贝转入患者的细胞,但被科学家寄予厚望的病毒没能很好地完成这一任务。到了20世纪末,病毒载体甚至还引发了一些意料之外的并发症。这使科学家意识到,要想解决囊性纤维化的基因问题,可能只有寻求其他办法。
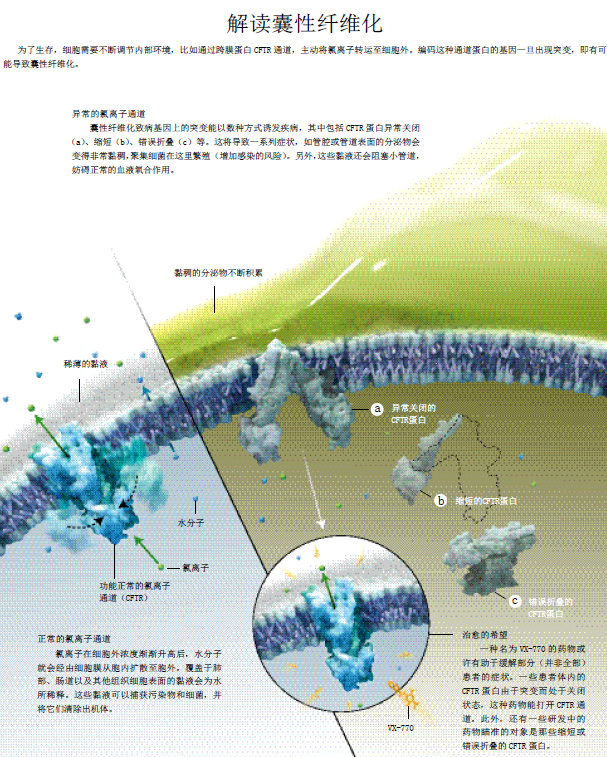
同时,一些细胞生物学家也在努力完成一项极具挑战性的任务:弄清楚正常蛋白是什么样子,它们的工作机制是什么,以及基因缺陷如何导致囊性纤维化。这就意味着,他们要在更加精细的层面上,研究正常蛋白的三维结构,对异常蛋白干扰细胞功能的各种方式也要有深入了解。不过,这些细胞生物学家所用的方法并不像基因疗法,需要把缺陷基因替换成正确基因,以产生正常蛋白,他们走了一条截然不同的路:寻找一种药物,纠正异常蛋白的功能。通过大规模搜寻找到的药物,或许能让囊性纤维化患者活得更久、更健康。
如今,这种平缓却稳妥的方法似乎成功在即。一些治疗囊性纤维化的新型药物已进入临床研究的最后阶段——其中有一种药物对特定患者尤其有效,很有希望成功。如果这种药物最终能成功上市,它将成为第一个针对囊性纤维化病理机制的药物,而不是仅针对表面症状。还有其他好消息。初步研究显示,这些候选药物或许还能对付其他常见疾病,比如支气管炎、慢性鼻窦炎、胰腺炎等。
疾病的根源
这些药物的发现之旅,始于科学家对囊性纤维化基本生物学机制的不懈探索。人们在很早以前就知道,这种疾病是由于人体特定组织中,氯化钠的跨细胞膜转运出了故障所致。这些组织中的细胞要把氯化钠中的氯离子转运到细胞外,以维持细胞内液与外液之间的电解质平衡。当氯离子在细胞外积累时,水分子也会向细胞外扩散。供氯离子出入的通道都是一些蛋白分子,细胞合成出这些蛋白后,就会把它们插入细胞膜,而后每个蛋白就将形成一个跨膜离子通道。
1989年发现的那种能导致囊性纤维化的基因就是编码这类蛋白,名为囊性纤维化跨膜转导调节因子(cystic fibrosis transmembrane conductance regulator,简称CFTR)。正常的CFTR分子约由1 500个氨基酸组成,氨基酸之间有着精确的排列顺序,它们会自我折叠,形成一系列三维的螺旋和片层结构,这些螺旋和片层结构又会作为构建单元,再次折叠,产生更加复杂的三维结构。氯离子可以通过离子通道进出细胞膜,而它们的流动,会使水分子也发生流动,有助于移除呼吸道,以及肠道、胰腺、肝脏等组织内部管道表面的黏液。此外,CFTR通道还可以转运其他一些离子,比如碳酸氢根离子(bicarbonate)。
问题就出在这里。基因突变导致机体缺乏正确的CFTR通道,以至于囊性纤维化患者产生的黏液又浓又稠,会干扰很多生理过程。在肺部,凝胶状的黏液会阻碍氧气向肺泡扩散,使得呼吸这样的简单行为也像“拉风箱一般”。不但如此,黏液累积多了之后,还会成为有害细菌(通常是铜绿假单胞菌,Pseudomonas aeruginosa)的繁殖温床,可能导致严重感染。在胰腺中,厚厚的黏液和久不清除的分泌物会堵住消化酶的分泌通道,使之无法经由各种管道进入肠道,干扰了正常的消化过程。由此产生的后果是,囊性纤维化患者的体重常常低于健康下限,而且大多伴有营养不良症状。同时,胆汁也淤积在肝脏处,无法正常处理的脂肪便会阻塞在肠道中,导致便秘,有时甚至会使整个胃肠道“罢工”,危及生命。
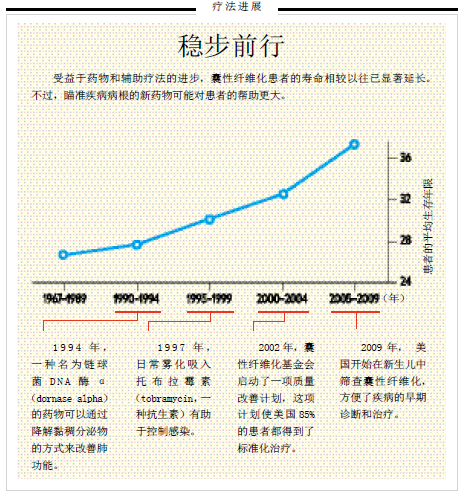
在对付肺部感染的抗生素以及更好的营养疗法面世之前,绝大多数囊性纤维化患儿在婴儿期便已夭折。过去数十年间,随着医疗技术和辅助手段的进步,患者的寿命已经有了实质性的延长。一些治疗手段非常简单,适合没有医学背景的人,比如让父母摇晃或拍打患儿的胸部,以便改变肺部黏稠分泌物的位置,让黏液不再堵塞肺部管道。一些药物则可以扩张呼吸道,抑制感染,或者有助于降低呼吸道黏液的分泌量。维生素和酶类可以帮助消化。在这些努力之下,大约一半的囊性纤维化患者能活过37岁,甚至更久。然而,没有一种疗法能直指病根,不能让足够的氯离子流向细胞外。
三种突变
要想找到一种药物,使氯离子通道至少恢复部分功能,科学家首先要做的是,在显微水平上摸清囊性纤维化发病机制的细节。遗传学家检测了世界各地患者的DNA样本,迄今已发现CFTR基因的1 600多种突变,都能导致严重的囊性纤维化。突变基因编码的CFTR蛋白能产生多种有害效应,可分为好几类,其中有三类研究得最为透彻:一是氯离子通道不能定位于细胞膜上(即细胞膜上没有氯离子通道);二是通道长度不足,而且用于指导蛋白合成的RNA分子很快就被降解掉;三是通道虽然长度正常,却无法开放,氯离子无法出入。针对某一种有害效应而研制的药物,在面对其他两种效应时通常难以奏效。因此,为了让所有囊性纤维化患者受益,科学家需要根据不同患者的情况,针对不同的发病机制研制不同的药物。
细胞表面完全缺失氯离子通道,是由最常见的一种基因突变导致的。该突变仅使CFTR蛋白的1 500多个氨基酸缺失了一个。这个缺失了的氨基酸名为苯丙氨酸(phenylalanine,常用字母F指代),在CFTR蛋白的氨基酸链上处于第508位,因此这类突变被命名为F508del(del为“缺失”之意)。
F508del突变会引起囊性纤维化,起初多少有些让人吃惊。尽管发生了这类突变,但细胞仍能把氨基酸依次连接起来,制造出一个氯离子通道,而这个通道也能在一定程度上执行氯离子的运输功能。然而,细胞自身的质量控制系统却不允许这件事的发生。在细胞内,存在着好几百个辅助蛋白和酶类,负责新生CFTR蛋白在细胞内的运输,监督该蛋白的折叠过程,并协助细胞,把CFTR蛋白插入细胞膜。在折叠过程中,哪怕出现一丁点儿差错,比如F508del突变引起的单个氨基酸缺失,也会被监控系统立刻识别出来,细胞随即就会摧毁突变蛋白。结果,尚保留着部分功能的氯离子通道连细胞膜都没碰着,就被宣判死刑。
由于F508del突变是囊性纤维化的最常见致病原因,世界上很多研究机构(包括我们)一直在研究,这种突变到底使哪个关键环节出错,以至于 CFTR蛋白成为“废品”,被细胞扔进 “垃圾回收站”。这类研究有助于寻找一些药物,通过纠正折叠过程,以免CFTR蛋白被细胞摧毁,从而在不影响细胞识别和清除其他异常蛋白的情况下,缓解囊性纤维化患者的病情。
弄清楚如何调节细胞的质量控制系统不止对囊性纤维化的治疗有好处。很多慢性病的发生,比如胆固醇代谢综合征和以抗胰蛋白酶缺乏症为代表的遗传性肺部疾病,都是由于蛋白质的错误折叠而导致的。至少在一些疾病中,越来越多的证据表明,导致疾病的真正原因并不能归咎于蛋白自身的功能改变,而是因为质量控制系统倾向于彻底降解异常蛋白分子,或者使它们变性、沉积,形成一个团块。可以想像,如果质量控制系统“高抬贵手”,饶恕这些蛋白,容许它们执行应有职能,那么很多只是稍微折叠有误的突变蛋白仍能发挥重要作用。由此可见,从细胞的质量控制系统着手,科学家既能对多种疾病有更深的认识,也可能找到更有价值的疗法。
世界范围内,约有10%的囊性纤维化病例是由CFTR通道异常缩短引起。而在以色列,这样的一种名为W1282X的遗传突变,更是与40%的囊性纤维化病例有关。由于突变基因含有错误指令,使得蛋白质在合成过程时,氨基酸链只延伸到第
1 282个氨基酸便提前终止。这个位置上的氨基酸通常是色氨酸(常用字母W指代)。致使蛋白质合成出错的指令叫做无义密码子(nonsense codon),它对蛋白质的正确合成其实有着非常重要的作用,但前提条件是,它要出现在正确位置上。在囊性纤维化病例中,CFTR的合成却被这个密码子提前终止。而且,直接指导合成过程的信使RNA也被细胞视作异常分子,给降解掉了。这样一来,即使错误的终止指令被忽略掉,也没法制造出功能完好的CFTR蛋白了。因此,治疗W1282X相关病例的药物可能需要同时解决两个问题,而不是一个。
最后一类突变是使离子通道无法打开,保持闭合结构,以至于氯离子难以通过通道流向细胞外。由此导致的囊性纤维化病例数约占全球的5%。在这类突变中,一种名为G551D的突变会引起特别严重的囊性纤维化。尽管每一种基因突变通常都需要一种针对性疗法,但科学家的研究表明,能使 CFTR通道打开的药物,也许还能治疗没有携带此类突变的患者。比如在F508del突变中,可以先用一种药物使少量CFTR蛋白插入细胞,再用第二种药物撑开离子通道。这样一来,就可在一定程度上让更多的氯离子,通过这些原本功能不大正常的通道流向细胞外。
药物何时出现?
在药物研制的漫长过程中,我们的第二步就是要寻找一些药物,用以缓解CFTR基因的特定突变所引起的种种病理效应。这一步从F508del突变开始应该是最明智的,因为它在囊性纤维化患者中最常见,而且这个突变基因所编码的CFTR蛋白还保留有部分功能。如果科学家能阻止该蛋白的过早降解,那么它们就可以发挥一定的作用,不需其他干预,肺部功能就会得到改善。
在F508del突变中,对于CFTR蛋白的折叠何以出错,细胞的质量控制体系如何检测折叠错误,科学家还远未弄清楚。不过,要想判断一种药物能否缓解错误折叠引起的病理效应,应该是很简单的。通过向细胞引入荧光分子,科学家就可以检测氯离子或其他离子进出细胞时引起的微弱浓度变化。当患者接受候选药物的治疗后,如果氯离子流出细胞,科学家就可以推断,异常CFTR蛋白恢复了部分功能。反之,如果氯离子没有流动,就说明药效不够,需要继续寻找更有效的药物。在自动化和计算机技术的帮助下,药物筛选可以快速进行,短时间内就能完成对数百万种药物的筛选。
美国Vertex 制药公司找到了一种药物,代号VX-809,虽然初步研究的结果很令人兴奋,但在人体试验中,对肺功能的改善却不明显。美国PTC医疗公司(PTC Therapeutics)则在对另一种药物进行临床试验。这种名为Ataluren的药物针对的是一类不太常见的突变,即CFTR蛋白缩短型突变。Ataluren可以让蛋白合成系统忽略错误指令,不会合成出不完整的CFTR蛋白。另外,还有些遗传疾病与无义密码子出现在不正常位置有关,如赫尔勒氏综合征(Hurler syndrome)、杜氏肌营养不良(Duchenne muscular dystrophy)等,科学家也在试验Ataluren对这几类疾病的效果。
目前,针对G551D突变的研究结果算是最好的。Vertex公司的科学家筛选了228 000种可使离子通道打开的候选药物,结果发现,有一种药物能够选择性地激活CFTR通道的能量开关,使该通道的功能恢复到正常水平的50%。这无疑是一个很不错的结果,这种代号为VX-770的药物正在经受大规模实验的考验。在临床实验中,VX-770能在数周内,使G551D突变型患者的呼吸功能得到实质性改善,而且这种效果能持续到实验结束(实验时间为一年)。同样重要的是,在治疗期间,患者住院次数明显减少,体重平均增加了7~8磅(1磅约0.45千克)。本文作者史蒂文·M·罗是美国首个让患者接受VX-770治疗的临床医生。在今年年底,Vertex公司打算向美国食品及药品管理局提交该药的上市申请。在进一步的临床研究中,VX-770在与其他药物合用的情况下,也显示出了较好的效果(亚拉巴马大学是Vertex和PTC公司试验新药物的合作单位之一。本文作者罗和克兰西为两家公司的药物研发都提供了一些建议)。
这些都是突破性的研究成果。一些直指囊性纤维化根源的候选药物的发现说明,几十年来,科学家对该病基础生物机理的研究终于取得了成效。尽管这些候选药物的安全性和有效性仍在经受更大规模的人体试验的考验,但我们有理由保持乐观:困扰人类已久的囊性纤维化终有一天会被“连根拔除”。
请 登录 发表评论