镇痛药的安全漏洞
撰文 加里·斯蒂克斯(Gary Stix)
翻译 褚波
由于阐明了人体产生前列腺素(prostaglandin)的生理机制,本特·萨穆埃尔松(Bengt Samuelsson)于1982年获得了诺贝尔生理学或医学奖。在人体内,前列腺素是一类重要的激素,调节着多种生理过程,比如引发疼痛、发烧、发炎,不过这些过程可以用阿司匹林、布洛芬等药物来抑制。与萨穆埃尔松合作研究、共享1982年诺贝尔奖的,还有另一位科学家——苏内·贝里斯特伦(Sune Bergstrom),两人的研究工作都是在瑞典卡罗林斯卡医学院的红墙校园内开展,每年诺贝尔生理学或医学奖的颁奖典礼,也都会在这里隆重举行。
在卡罗林斯卡医学院,关于前列腺素的故事可以从1930年发现脂肪酸开始,一直讲到今天。最近几年,萨穆埃尔松与合作者一起,进一步弄清了前列腺素的生物化学性质。这是一项基础性研究工作,利用前列腺素的生物化学性质,就可以开发出比现有药物(如逐渐被弃用的COX-2酶抑制剂,具体内容参见《环球科学》2006年第7期《告别疼痛》一文)更安全的镇痛、消炎药物。萨穆埃尔松说:“消炎药物的需求量很大,开发出效果不比以前的药物逊色、副作用却更少的新型药物非常重要。”
发现新目标
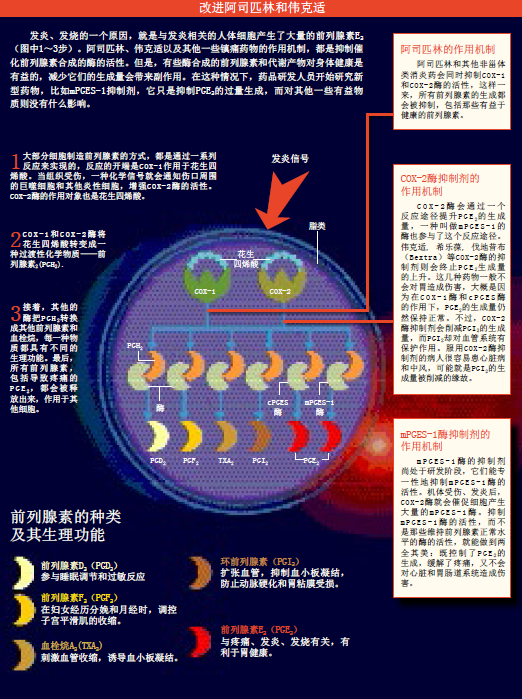
1982年,卡罗林斯卡医学院为萨穆埃尔松获得诺贝尔奖专门发布了新闻稿,高度评价了他的研究工作,因为他把前列腺素的方方面面都诠释得尽善尽美。萨穆埃尔松在试验中发现,只要细胞膜上的花生四烯酸(arachidonic acid)与酶在不经意间相遇,就会发生一系列生化反应。最终产物就是各种类型的前列腺素,它们能调节人体内多种生理功能,比如促进肾脏的血液循环;在妇女经历分娩和月经时,控制子宫肌肉的收缩;在人体受伤或被感染后,引发炎症反应(特征是伤口周围又红又肿),保护机体免遭损害。
阿司匹林和其他一些非甾体类消炎药物(如布洛芬),会在前列腺素合成途径中的前几个步骤,抑制1型和2型环加氧酶(COX-1和COX-2)的活性,达到镇痛消炎的目的。但是一旦抑制了环加氧酶的活性,就等于切断了所有类型前列腺素的合成途径,机体便无法合成任何前列腺素。
正是由于上述原因,阿司匹林以及类似药物会导致很多问题。阿司匹林既抑制了引发炎症反应的前列腺素的产生,也会削减其他类型前列腺素的产量,比如帮助胃粘膜对抗消化液中的盐酸的前列腺素。为了解决这一难题,20世纪90年代,一些制药公司提出了一项补救方案,他们开发出伟克适(Vioxx)、希乐葆(Celebrex)等药品,专门抑制COX-2的活性,而对COX-1没什么影响,这样就不会干扰胃保护性前列腺素的产生。
但科学家很快就发现,抑制COX-2的活性也不是一个十全十美的解决方案。COX-2的活性受到影响后,前列腺素之间的一系列复杂反应都会受到明显干扰。虽然抑制COX-2的活性能削减前列腺素E2(PGE2)的生成量,缓解疼痛、防止发炎,但也会抑制环前列腺素(prostacyclin,PGI2)的合成,而PGI2却是一类有益于心脏健康的前列腺素,它能促进血管扩张,阻止血小板凝聚。所以,让病人服用COX-2抑制剂来缓解疼痛,无异于饮鸩止渴。
1999年,美国宾夕法尼亚大学医学中心的加勒特·A·菲茨杰拉德(Garrett A. FitzGerald)在《美国国家科学院院刊》上发表了一篇文章,报道了一项小型临床试验的结果。在试验中,他抑制了PGI2的合成。菲茨杰拉德发现,病人服用COX-2抑制剂(血栓烷)后,虽然PGI2的生成量会减少,但与此同时,在花生四烯酸途径中合成的另一种前列腺素仍在发挥作用,而且它的作用是与PGI2相互克制的,也就是说,它会促进血管收缩和血小板凝聚。PGI2的含量下降以后,血液中的平衡就被打乱了,血液很容易凝结,形成血栓,继而导致心脏病和中风。近年来,因为COX-2酶抑制剂引起的医疗事故,律师为起诉人状告制药公司的案例屡见不鲜。菲茨杰拉德初次报道自己的研究发现,是在1997年一场学术会议上,也就是第一种COX-2抑制剂——希乐葆获准上市的前一年。
菲茨杰拉德的研究小组最先把暗藏在COX-2抑制剂中的危险公之于众,不过,萨穆埃尔松的研究小组不甘落后,也有了新发现。佩尔永汉·雅各布森(Per-johan jakobsson)是萨穆
埃尔松实验室的一位博士后研究人员,他领导的实验项目在人体中发现了一种可以生产PGE2的酶。1999年,雅各布森、萨穆埃尔松以及两位合作者共同发表了一篇文章,他们在文章的摘要中说道:“这种酶很可能是一个新的药物靶标。”
萨穆埃尔松实验室的研究成果引起了一家小型制药公司的注意。这家公司名叫Biolipox,由卡罗林斯卡医学院的两位科学家创办。2000年,该公司涉足呼吸道疾病消炎药物的开发领域,研制出了eoxin。这种生化物质也是在花生四烯酸途径中合成的。2001年,Biolipox公司决定扩充药品种类,实现产品多样化,于是它从卡罗林斯卡获得了雅各布森发现的酶(微粒体前列腺素E合成酶,英文缩写为mPGES-1)的知识产权。能选择性地抑制mPGES-1的活性的药物,也许就能镇痛消炎,而不会引发胃肠道或心血管疾病,因为它们不会降低PGI2在血液中的含量。Biolipox公司的首席科学家夏洛特·埃德纽斯(Charlotte Edenius)说:“我们意识到,这种药物将是第三代非甾体类消炎药物。”
在竞争与质疑中前行
Biolipox公司的总部设在卡罗林斯卡医学院的校园内,公司大楼是一栋朴实无华的建筑物,学校的科学图书馆和生物信息学教学部也在里面。萨穆埃尔松既是公司的科学顾问,也是董事会成员。勃林格殷格翰(Boehringer Ingelheim)公司是COX-2抑制剂——Mobic的制造商,它在2005年与Biolipox公司签了一份合约。合约中规定,勃林格殷格翰公司为Biolipox公司提供资金研发mPGES-1抑制剂,研究成果与市场销售权则归勃林格殷格翰公司所有。
在美国的药物市场上,非麻醉类镇痛药的销售额每年超过100亿美元,这也就意味着,其他制药公司也会对mPGES-1虎视眈眈。默克公司已经发表了一项关于mPGES-1抑制剂的研究成果,辉瑞公司则为一只小鼠申请了一项专利,他们把小鼠体内编码mPGES-1的基因敲除掉,这样就能很直观地看到mPGES-1的活性被抑制后会有什么样的后果。其他制药巨头也相继申请了与mPGES-1有关的专利。菲茨杰拉德说:“药物市场变幻莫测,对于目前任何一种药物,巨大的市场背后都隐藏着不安全的因素。”他还补充说,有一家公司(他不愿意透露具体名称)准备在2007年将他们的mPGES-1抑制剂推进到临床试验阶段(另外,还有一些公司在开发能与PGE2受体结合的药物,这样就可以直接让PGE2失去作用)。
伟克适等药品带来的教训也许能制止其他消炎药物匆忙上市。其实一些持怀疑态度的人已经开始质疑了。2006年,《药理学趋势》(Trends in Pharmacological Sciences)发表了一篇文章,题为《mPGES-1真有希望成为消除疼痛的靶标吗?》。文章提出了一大疑问:前列腺素代谢过程的复杂性是否会让新镇痛药败走麦城?文章还评论说,抑制mPGES-1的活性也许能降低PGE2的浓度,但其他种类前列腺素的含量却会因此上升,这会带来什么样的生理影响,谁都不清楚。更何况除了PGE2外,其他前列腺素也能引发疼痛。
似乎只有人体安全性和药效性试验才能平息一切争论。不过,早期的小鼠试验带来了些许希望。2006年,菲茨杰拉德的研究小组发表了一个报告,他们敲除了小鼠的mPGES-1基因后,对心脏有益的PGI2的含量增加了,而有害的血栓烷的含量则没有发生什么变化,小鼠的血液没有出现异常的凝结现象,血压也很正常。菲茨杰拉德的研究小组接下来又进行了一些试验,结果证明小鼠的心血管因为mPGES-1的消失而越发健康,也许这是因为PGI2的含量升高的原因吧。
对镇痛药物的研究仍在继续,新的药物需要像敲除mPGES-1基因一样,不仅能镇痛,还要能保护心脏、促进健康。科学家和制药公司都准备好了,他们将告别小鼠实验,进军人体试验了。
请 登录 发表评论