被誉为“终极干细胞”的iPS细胞的登场,令人意外地推动了“不使用干细胞”的研究再次活跃起来。
山中博士团队所开发的细胞初始化方法的关键,就是把那些在分化的细胞中活动比较活跃的、被称为“转录因子”的基因,人为地使其在分化后的细胞内活跃起来。DNA中含有的基因种类超过2万种,哪些基因会被读取并发挥作用,影响着人类细胞的性质和状态,而这基本上是已经决定好的。转录因子,就相当于决定其他基因活动方式的“指挥部”。山中博士的团队挑选出大概100种在ES细胞中活动活跃的基因,并最终筛选出4种转录因子,通过它们的活动,诱导皮肤细胞成为与ES细胞相似的状态。
实际上,少数的基因决定了细胞的种类,这种观点自很久之前就一直存在。1987年发表的一篇论文显示,如果向白鼠的皮肤细胞中加入一种转录因子的基因的话,该细胞就会转化为骨骼肌细胞。据说,1990年之后,寻找决定细胞种类的“关键基因”的研究,曾经进行得如火如荼。
之后,这项研究逐渐降温,但是山中博士的成功使之又活跃起来。石井博士说:“从20世纪60年代开始,人们就考虑过几种初始化细胞的方法,或将某种细胞转化成另一种细胞的方法。山中博士团队的成果的意义,就在于它表明了使用转录因子的方法是最有效的。”此外,日本九州大学的铃木淳史教授回忆说,“当听到山中博士的研究时我就想,按照同样的思路,分化后的细胞之间应该也可以直接转换”。
在特定情况下,直接转换也可用于治疗
山中博士团队的成果发表以来,“向某种细胞内注入少量转录因子的基因,该细胞便可以直接转换成另一种细胞(俗称‘直接复制’)”的各种研究报告,也相继发表了。
比如研究人员发现,向白鼠的皮肤细胞中放入3种基因的话,它就会转换为心肌细胞,放入另外3种基因则会转换为神经细胞。2011年6月,铃木博士的团队向白鼠的皮肤细胞中注入两种基因,将其成功地转换为了肝细胞。
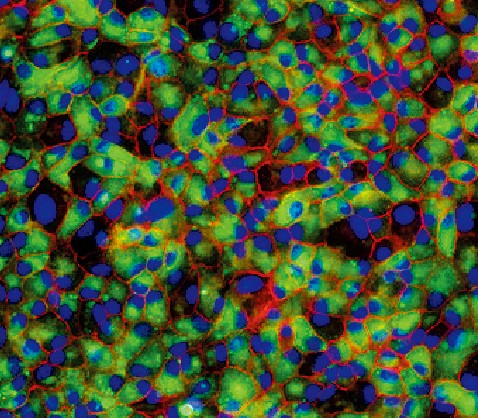
通过直接转换培育的肝细胞
直接转换白鼠的皮肤成纤维细胞培育的肝细胞(上皮细胞的一种)群。使可以发出荧光的分子与各个细胞内的蛋白质结合,然后用荧光显微镜拍摄。绿色部分表示的就是肝细胞内的蛋白质。此外,红色表示的是上皮细胞内的蛋白质,蓝色表示的是细胞核。
虽然大多数情况下,不用病毒就不能直接转换,但是也不断有动物实验表明,通过直接转换培育的细胞也可以用于治疗。甚至在医疗应用上,直接转换所拥有的一些优点,还是iPS细胞所没有的。
首先,培育出目标细胞所需的总时间很短。在使用iPS细胞时,从患者的皮肤等细胞培育出iPS细胞就至少需要一个月的时间,将该iPS细胞进一步培育成目标细胞或组织就更花时间了。对于脊髓损伤或急性肝炎这种分秒必争的情况来说,这是来不及的。如果有“iPS细胞银行”来事前储备用于培育治疗用的细胞或组织的iPS细胞的话,倒是可以缩短培育时间,但现在还不能实现。
此外,直接转换培育出的细胞的“纯度”较高,这对于移植来说是很有优势的。由于iPS细胞几乎可以培育出任何一种细胞,所以在让它转换为目标细胞的过程中,也会产生一些不需要的细胞。如果移植了这样的细胞或者没有转换为目标细胞的iPS细胞的话,最坏的情况就是可能有癌化的风险。而直接转换的话,几乎不会产生不需要的细胞。
但在另一方面,直接转换难以确保得到所需的细胞数量,因为这样培育出来的神经细胞或心肌细胞并不会增殖。据说,要想得到满足治疗要求数量的细胞,需要若干平方厘米的皮肤才够。
相比之下,iPS细胞的增殖能力强,想得到大量目标细胞时,它的优势就比较大。此外,在人类或白鼠的内脏器官中,肝脏是惟一可以再生的,它比较特殊,所以通过直接转换培育的肝细胞也可以再生。但是据说,要将人体的细胞成功地直接转换为肝细胞还需要时间。
“对于一些疑难症的患者,直接转换可以缩短治疗时间,这一点对于iPS细胞来说确实有优势。我想,还是需要根据时间和具体情况来选择使用哪种方法。”铃木博士说。
iPS细胞不仅开辟了通向新医学的大道,也推动了细胞直接转换的基础科学研究。在下一期中,我们将走向使用iPS细胞制药及临床研究的最前沿。此外,还将介绍在保存稀有物种等方面,正在逐渐拓展的iPS的其他非医疗应用。
(本文发表于《科学世界》2013年第1期)
请 登录 发表评论