组装生命的学科
合成生物学(Synthetic Biology)一词最早出现于1911年,而真正发展成为一门学科则是在2000年。随着分子生物学、系统生物学、生物信息学等的迅猛发展,人类对于生命的理解越发深入,对细胞和分子的结构和功能细节的了解也开始变得清晰,在细胞和分子水平的生物学操作越来越得心应手。
就像小的时候一遍又一遍拆解收音机,终于有一天,我们开始购买零部件,尝试自己组装一台与众不同的收音机。在合成生物学中也有类似的常规研究策略,可以分成两种操作方式。第一种是对现有基因进行更改,去掉、替换或是添加新的序列,是在生命系统的基础上进行的操作,我们称之为“自上而下法”;与之相对的“自下而上法”属于第二种,它对无生命的原料组分进行操作,来重建生命系统。
虽然策略不同,但科学家们都希望能够设计并合成出自然界不存在的、具有预期功能的生命系统。因此,与其说这是生命科学自身的重大进展,倒不如说是生命科学与工程学的交叉,“工程师们”将他们熟悉的设备零件换成遗传材料,按照“合成”的理念,根据策略和技术方案重新进行组装。如果说,基因工程是“读DNA”(如克隆或测序),那不妨说合成生物学是“写DNA”。
对生命的各种改造
早在2002年,纽约州立大学维默尔小组的塞洛等人,就制造出了历史上第一个“人造生命”—人工合成的脊髓灰质炎病毒。这一工作开创了以无生命的化合物合成感染性病毒的先河。
合成生物学研究的典范之作,当属加州大学伯克利分校教授科斯林采用合成生物学的方法生产青蒿素。青蒿素是我国首先发现的抗疟疾良药,它挽救了全球数百万人的生命,在世界医药界占有重要地位,其发现者—中国中医研究院(今中国中医科学院)中药研究所的屠呦呦,也因此获得了2011年度拉斯克临床医学奖。
青蒿素一般通过植物来提取,但产量很低,成本也高。科斯林教授尝试着构建一个生产青蒿素的细胞加工厂。他的研究团队将来源于青蒿的紫穗槐(青蒿酸)合成酶基因和一些相关的酵母基因转入大肠杆菌,并成功启动了酵母甲羟戊酸途径,重新改造合成路线后,便可大量生产青蒿素的前体。随后,他们的团队又瞄准了酵母,构建了与大肠杆菌相似的代谢通路,改造了酵母自身的甲羟戊酸途径,让酵母菌生产青蒿酸,大大提高了青蒿酸的合成能力。
这一工作,完美地展现了合成生物学的魅力。通过人类的操作,成功解决了来自大肠杆菌、酵母、青蒿多种基因及其代谢途径的组装与精密调控工作;同时,优化发酵工艺,还可进一步提高产量。科斯林对它的前景非常乐观,“如果你用大约10万升的发酵槽来生产酵母、产生青蒿素,一直运作下去,就可以为全世界生产出足够的青蒿素”。
文特尔和人造生命
合成生物学真正引起大众的关注,始于文特尔(J. Craig Venter)。他的扛鼎之作“人造生命”,不仅是合成生物学领域的最大突破,也震惊了全世界。
实验中,科研人员合成了蕈状支原体(Mycoplasma mycoides)的DNA,然后将它移植到山羊支原体(Mycoplasma capricolum)的细胞中。如此一来,就有了一个全新的细胞,“披着”山羊支原体的“皮”,却有着蕈状支原体的“心”。如果到此为止、仅仅是看起来很像,那显然不是科学家的目标。经过成千上万次尝试,新注入的基因组终于成功取代了原有的基因组,细胞产物都是蕈状支原体的产物,新细胞也开始在培养皿中生长、繁殖,产生了一代又一代的人造生命。文特尔将这个小小的“人造生命”称为“辛西娅”(Synthia),也就是“人造儿”的意思。
这一过程,同样体现了合成生物学的标准工作模式,可分为两个步骤:一是合成基因组;二是将这个基因组植入异种细胞中,并使其顺利表达期望的产物。这个研究历时15年。为了证明它是合成的结果,研究人员特意在合成基因上留下了“水印”,包括全部46名科研人员的姓名和研究所的网址,以及一句名言:“生存、犯错、倒下、战胜,用生命创造生命。”
酵母生产青蒿素和人造生命“辛西娅”,堪称合成生物学的大师经典之作。与此同时,也有很多科学家在进行着一些虽不瞩目却也很有意义的研究。
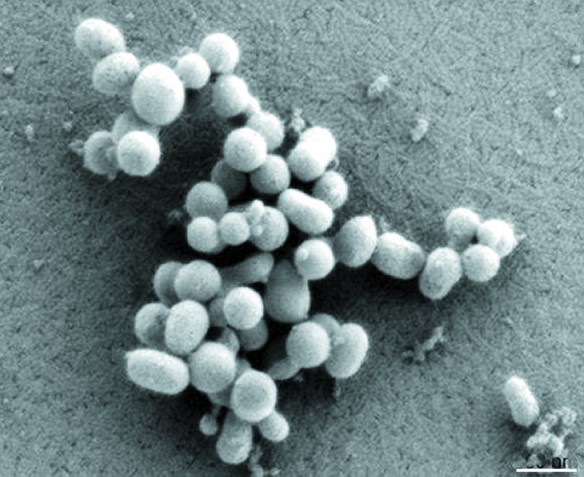
这幅电子显微镜照片显示第一个被植入了人造DNA的细胞—“辛西娅”正在增殖的情形。图中标尺为500纳米。
(本文发表于《科学世界》2013年第1期)
请 登录 发表评论