价电子是原子之间的粘合剂
原子性质主要是由最外层电子数量决定的,它们往往“追求”2、8、18⋯⋯的稳定状态,也可以说是“完美”状态。外层电子较多的接近“满态”的原子“希望”得到电子,碰到别的原子时得不到别的原子的电子就与其共用电子,形成共价键;能夺得电子时,就干脆抢得电子形成负离子。正好有些原子外层电子较少,“无望”得到多个电子,那就“舍弃”外层电子,成为正离子,与负离子以离子键形式结合。典型的例子就是氯原子碰到钠原子,组合成氯化钠分子。
实际上,离子键的情形也是当2个原子靠近时,未配对的单电子的电子云相互重叠,形成1个新的电子云,只不过这个新的电子云更靠近外层电子较多的原子,几乎被这个原子所独占。
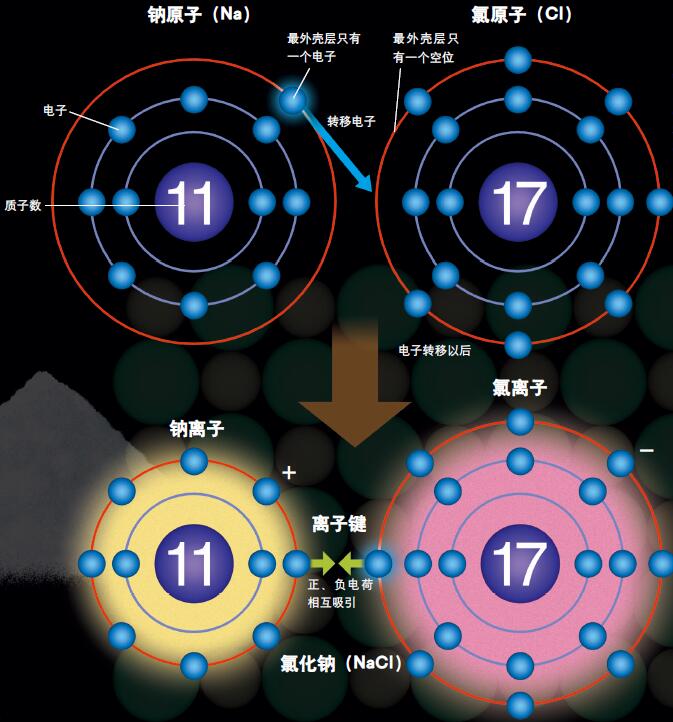
食盐的形成方式
钠原子的最外壳层上只有一个电子,氯原子的最外壳层上正好有一个空位。从钠原子向氯原子转移一个电子。钠原子和氯原子分别变成带正电荷的钠离子和带负电荷的氯离子,两者相互吸引结合在一起,形成氯化钠。图解中的背景绘图表示的是氯化钠固体中的原子排列。
当外层电子都较少的原子靠近时,它们会“舍弃”外层的电子,形成满壳层稳定状态,电子则成为在原子之间运动的“自由电子”。自由电子也相互配对,处于不同的能级,分布在失去电子的晶格状密排的原子之间,形成所谓“电子海”,把原子(实际是离子)吸引在一起。这就是所谓的金属键,这样组合起来的原子显示出金属性。能够形成金属键组合的原子称为金属原子。
一般金属都是由大量的原子组合在一起,整体显示出金属性质。实际上,2个金属原子相互靠近可形成1个金属分子,3个原子可形成3原子分子,n个原子可形成n原子分子。其中的自由电子像“胶水”一样,把原子们粘合在一起,形成原子晶体。
在原子的结合过程中,价电子起到关键的作用,一般情况下,它们成单的电子需要“婚配”成对(自旋相反),产生出原子间的结合力。但关键不在于电子成对,有时电子不能成对也会在原子之间形成结合力,关键在于电子云的分布。比如氢分子失去1个电子,只剩1个电子,成为2个氢原子的离子(H2+),1个电子在2个氢原子核之间构成1个电子云,把2个氢原子核吸引在一起,表现出相对稳定的状态。
原子之间的结合可以说是多样的,也是复杂的,结合式样稍有差别,物质就表现出不同的性质,这也为什么我们见到的物质世界千差万别的原因。
原子基本没有单独存在的
较轻的原子核聚在一起,在一定条件下会自发地进行核聚变,组成较大的原子核,释放出能量,这个过程是朝向能量降低的方向发展,以求更加稳定。原子也一样,设想当初宇宙中某个地方因恒星演化生成各种原子的原子核后,逐渐冷却,原子核俘获电子变为原子,进一步变冷后原子也要相互结合在一起,释放出能量,保持稳定状态。这个地方就变成地球现在这个样子,有同种原子组成的分子或单质,更多的是不同的原子组成的化合物。如氧原子,生性活跃,与大部分原子都可形成氧化物或原子团,地球早期的物质中几乎没有单独存在的氧(单独存在也是少量的氧分子),究竟与什么原子组合是个复杂的长期演变的过程。只是后来有了光合作用,地球上单独的氧(分子)才多了起来。
但有一些电子填满壳层的原子,如氦、氖等稀有气体(曾经被称为“惰性气体”,因为特别“懒惰”的缘故),表现出极其稳定的性质,几乎不与其他原子交往,因为本身电子最外壳层已经排满,它们没有成单的电子,没有电子配对的“愿望”,这也是它们在极低的温度下也保持为气体的原因。
除此之外的其他所有原子之所以要组合起来,因为它们都有未配对的电子,“渴望”与其他有未配对电子的原子结合,达到相对稳定的状态。所有原子按照一定规则结合在一起,有的2、3个,有的4、5个⋯⋯构成1个稳定的分子或原子团,有的大量的原子组合在一起构成原子晶体。从某种意义上说,几乎任何两个原子都可以相互靠近,拉起手来,要么构成单质,要么构成化合物。
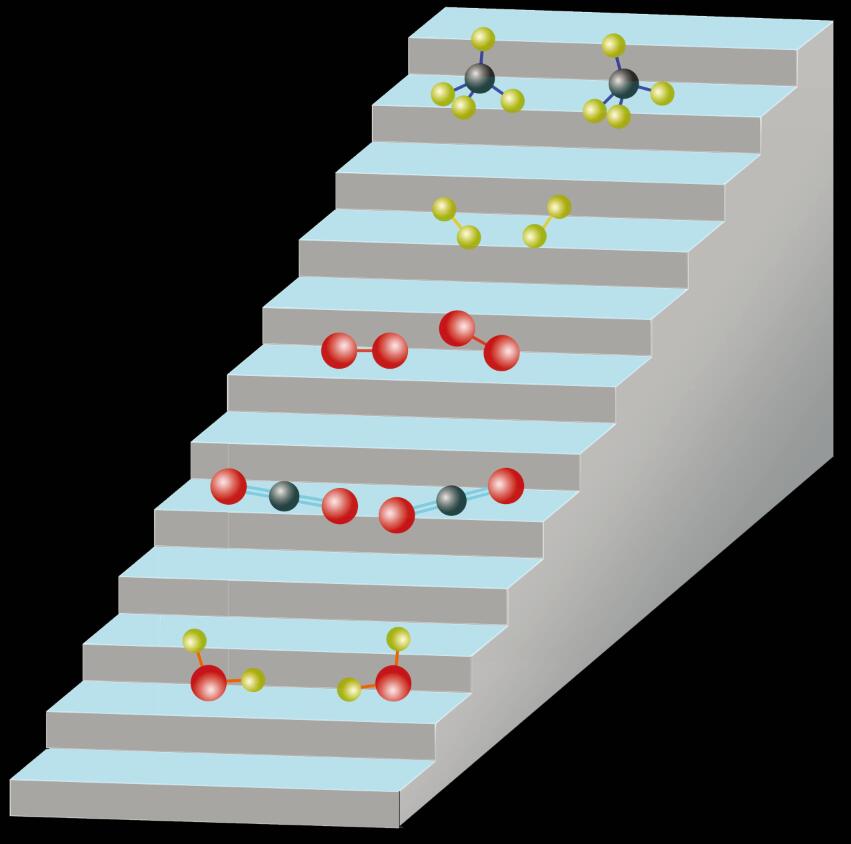
分子的稳定性由它的结合能决定
原子结合成分子只是达到一种相对稳定的状态,或称“亚稳态”,它们还有与其他分子或原子进一步组合,形成更稳定分子的趋势。它们寻求稳定状态的过程,是释放能量的过程,可以自然发生。在特定情况下也可吸收能量向上达到不太稳定的状态,比如更稳定的水分子分解为不太稳定的氧分子和氢分子。这里画成台阶状,更形象的比喻应该是一座大山上的一个一个山洼,山洼里的分子要分解的话需要一定的能量跃出山洼,就可与其他原子或分子发生化学反应,到达更低或更高的山洼,也就是变得更稳定或更不稳定。图中只是示意。
虽然原子相互结合构成了稳定状态,表现出不同的物质形态,但也只是相对的稳定。就像一座山包,沿着山坡有许许多多的平台,物体越往低处势能越低,也越稳定。这些单质或者化合物就像处在这高高低低不同的平台上,保持相对的稳定。它们在自然过程中总体有向下滑动的趋势,寻求更稳定的位置。原子在结合时释放出的能量越多越稳定,比如氢分子和氧分子都处在能量相对较高的稳定态,当它们结合成水分子时,要进一步放出能量,水分子就下降到更稳定的位置,与其他物质发生化学反应的难度增加了。
自然界中因为有能量的流动,所有物质都处于不断变化之中,原子之间的组合也是分分合合,没有真正达到“谷底”不再变化的物质,所谓不朽的东西实际上是处于能量更低更稳定的状态。
请 登录 发表评论