仿照结缔组织内氨基酸合成的氨基酸链,能够将热和化学能转化成动能。
活的生物体的运动是一种令人迷惑不解的现象。眨眼、肌肉痉挛、跑步运动员的突然加速、举重运动员的举重,看来都是自发地来自于生物体内部的力。它们不像喷气机、火箭或卡车的运动那样,利用的是髙温气体迅速膨胀所发出的推力,它也不像大帆船的航行、波浪的生成和风吹树动那样,是由外部施加的力推动的。

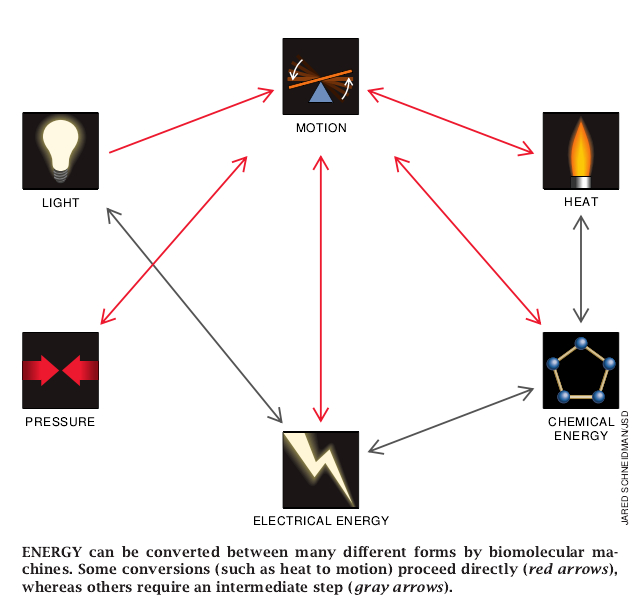
每一个活的生物体代表许多生物分子机构的成功集合,它能够将光能或原始化学形态的能量转换成生物体所需的各种运动、热量或用来建造和分解内部结构。在过去的40年间,生物化学家们已反过来建造了形成这些机构的主要成分的蛋白质模型。最近,我的同事和我取得了进展,可以设计能够进行在活的生物体中发生的能量转换的人工模型。这些有弹性的分子能够随化学信号和电信号而伸缩,它们或者能够随机械刺激而产生化学(信号)的输出。在理论上,这些分子能够把任何刺激转换成其它形式的能量。
合成的生物分子机构能够模拟特定蛋白质的功能,但它们要简单得多。由于它们削减了一些不必要的组件,所以它们能够使生物学家们更好的了解基本的细胞机制。实际上,我相信了解它们运行的原理就可以担负起生物能量转换的整个工作。
这些分子在医学和非医学应用方面还具有巨大的潜力。它们能够传递药物,阻止痕瘢组织的形成或吸去皮肤上的药液。进一步开发它们可能会预示一种新的伺服系统的出现,它将热、光、压力或化学变化的传感器与运动能力结合在一起。
在25年前,我的同事和我开始着手以前英国布里斯托大学的Miles Partridge(他最早分析了结缔组织的弹性结构蛋白)所从事的研究。我们提纯了弹性蛋白(这是在动脉、韧带、肺和大多数哺乳动物皮肤内发现的一种蛋白质),并发现了含有一种特定片段,即α弹性蛋白的溶液,随着我们把温度升高,此α弹性蛋白经历由无序状态向比较有序的状态转变。这些分子在15-25度摄氏度之间结合成致密而粘稠的样相。
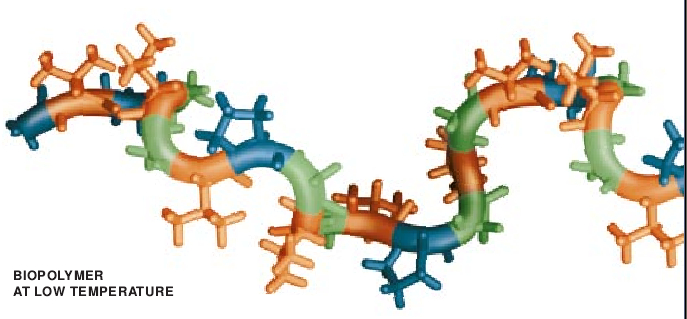
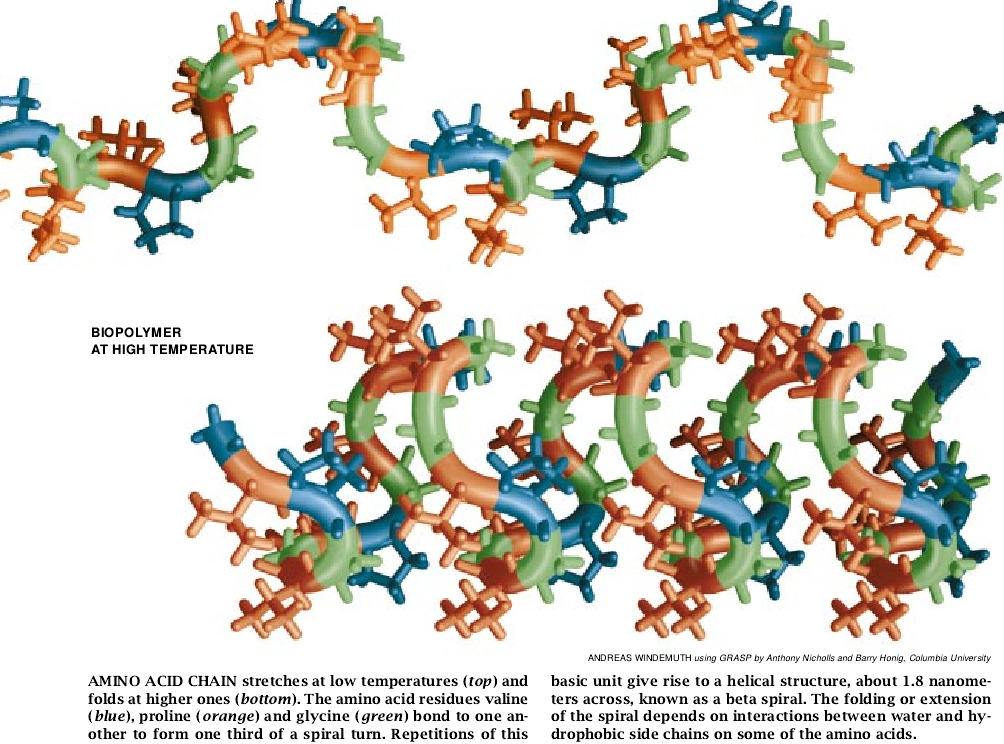
所有蛋白质都是连接的氨基酸长链,它是构成生命的基本单元(氨基酸本身是由附着于其上的侧链来区别的碳-氮骨架所组成的)。1973年,William R. Gray和Lawrence B. Sandberg以及他们在犹他大学执教的合作者发现了含有重复氨基酸顺序的弹性蛋白,这些氨基酸顺序中有缬氨酸-脯氨酸-甘氨酸-甘氨酸(VPGG)和缬氨酸-脯氨酸-甘氨酸-缬氨酸-甘氨酸(VPGVG)。自此以后,我们已经合成了由这些单元和其它重复单元组成的聚合物,并分析了它们的结构。用其它氨基酸残基,如谷氨酸(B)、赖氨酸(K)或异亮氨酸(I)来取代一个缬氨酸残基则得到具有某种程度不同性质的有关片段(VPGEG、VPGKG或IPGVG)。把这些片段掺入链中就能够改变该键的行为。
我们发现,合成的聚合物链就像它们的天然样本那样,开始呈伸展状态,接着随着温度的升高而呈螺旋状。继而这些螺旋聚合形成丝状体,该丝状体的大小与提纯的天然弹性蛋白相同。正如在此之前由博杜瓦大学的Laurie Gotte及其同事们所精确测定的那样。
当我们将这些聚合物分子交联成薄片或带状物时(用钴60产生的伽马射线照射),它们的举动非常相似于橡胶片的样子。特别是它们所显示的弹性几乎就是物理化学家们称之为熵的东西。有限的弹性在拉直原子间键的细金属丝中就能看见,当变形的力量消失时,键又把原子结合在一起,使细金属丝又恢复到原有的长度。可是,也可能由于过度拉伸而会断裂这些键。相反,当橡胶状的蛋白质被拉伸时,它们的骨架原子之问的键仍然未被拉伸,而是围绕着这些骨架键的其它原子的扭转运动受到了限制,因此整个分子变得比较有序。当把变形的力量移走时,熵——天然倾向于失序——就使这些分子恢复到它们的原有的较自由的排列。
我们大家都提出了证据,熵的弹性是可以恢复原状的。人体动脉的弹性纤维——特别是在主动脉弯曲处——通常以存活60多年而论,则要进行数十亿次的伸直和弯曲。
这些弹性聚合物的熵性质还提出了一个有关它们的特性的难题:它们的结构随着温度升高怎样变得比较有序的呢?大多数材料在高温下都变得不大有序,例如采用熔化或蒸发的方法。为此,我们把聚合物的变化视为一种逆温的相变。
我们认为,对这种现象的解释在于穿透进聚合物的水中。部分聚合物的链是疏水的(憎水),而另一部分链则是亲水的(喜欢水);于是水分子自身以不同的构型围绕这些分子的断面排列。这些构型的相对稳定性随温度而变化,从而蛋白质的择优形状也随温度而变化。
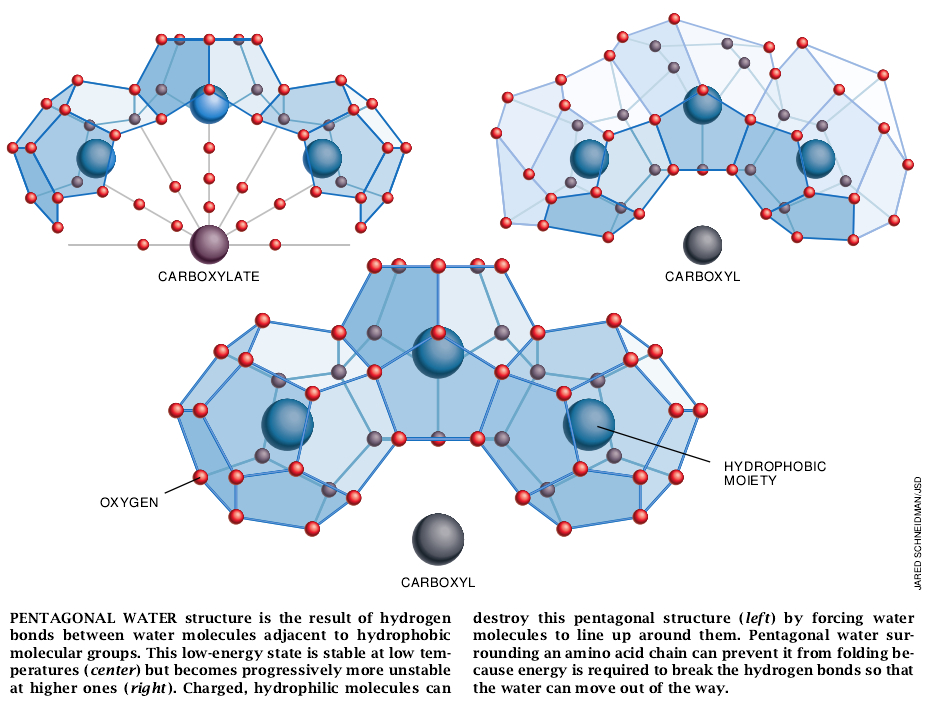
由于疏水的片段与水的相互作用不稳固,挨近疏水片段的水分子之间自身形成氢键,产生出一系列的五角形结构。水的这种排列有助于保持聚合物形状的延伸:折叠就需要断裂一些氢键。
有序的五角形结构在低温时是稳定的。可是,随着温度上升则有可能趋于失序,而在某些点上,随机的水分子热能则足以使氢链断裂。于是,水分子的五角形排列为无定形的、表征大量液态水的移动的氢键所代替。受水围绕蛋白质的阻挠,蛋白质也许就能够折叠成形。根据热动力学第二定律的要求,无序水的增加要超过有序链的增加:该系统的总熵升高了。
为把这种机制用于推动做功,我们把有弹性的薄片或带放进水浴中,把温度升高到这样的范围,即我们所期望的发生逆温转变的范围,正如我们所预料的那样,这些材料的膨胀长度的一半已收缩。通过随温度变化的运动,这些生物聚合物已将热转换成功,正如传统的发动机所作的那样,这种转换原来是有很高的效率的:有些生物聚合物能够将它的干重提高1000多倍。
发生转换作用的精确温度取决于聚合物内极性片段和非极性片段的混合,氨基酸上的亲水侧的键有助于升高转换的温度;而氨基酸上疏水侧的链则有助于降低转换的温度。这种趋势的原因是像羧基(COO-)这样的亲水基团对水分子施以大的拉力,所以能够破坏围绕在五角形结构水周围附近的疏水一侧的链,因此,得以破坏围绕着许多疏水基团的水的次序的温度。当亲水链存在于附近时,它将不大起作用,因为水已经失序了。
把亲水基团加到链上,由此而增加转换的温度。可是,同时亲水基团也降低了折叠所需的能量总量,这是由于只有少数残存的五角形水的键需要加以破坏,在一个生物聚合物中,每100个主链氨基酸残基正好插入二单元的羧基,能够把折叠所需的热总量降低75%。
当然,当动物运动时,它们的肌肉对电化学信号产生应答,不会有温度变化。为模拟此种行为,我们已制成了我们原有的生物弹性聚合物的变异体,该变异体受转换温度的改变的刺激能够引起折叠或打开。热环境保持不变,而分子的链则随温度变化而变化。我把这种效应叫做△Tt机制,是因为它以这种方式利用转换温度Tt。
这种技巧的关键,是氨基酸所具有的侧链能够把它的疏水行为改变为亲水行为(或者颠倒过来),这取决于围绕它的环境条件。我们最早成功地得到了在酸性条件下其侧链采取COOH形式、在中性pH下采取COO-形式的谷氨酸。COOH比带电荷的更疏水,所以在体温下含有谷氨酸的键应该在低pH时收缩,而在大致接近中性pH时膨胀,这在活的生物体内是普遍存在的。
我们用由聚合[4(VPGVG),(VPGEG)]制成的薄片证实了这种行为,该聚合物中的每5个重复的氨基酸序列中的一个在缬氨酸位置上含有一个谷氨酸残基。当我们把pH值由7变到4时,薄片收缩并增加了重量。据我们所知,这项实验标志着第—次合成的模式蛋白质已使化学能可逆地转换成运动。
由于纯粹是用温度来驱动转换,所以折叠发生的化学条件决定于亲水侧链和疏水侧链的混合。如果聚合物的侧链大多数是疏水的,那么大量的五角形水结构,在链能够收缩之前必然遭到破坏,其所需的能量能够把这种转换变成高的pH值。例如,如果谷氨酸被几个非常疏水的基团所包围,那么在普通体内的pH下,它的侧链仍会处于COOH状态。不过,这种转换作用一旦开始,将在小得多的pH范围内去完成。pH值由7变到8时,全部COOH基团将变成COO-(而不是通常使用从4变到7的pH范围)。
我的设想得到验证之后,我们能够使蛋白质链随受转换温度影响的任何可逆的变化而扩展或收缩。例如,我们能够通过把所谓辅基(实际上是一种可吸收或释放电子的分子片段)附着到此种链上来将电能转换成运动。辅基在其获得电子后的还原状态比其处于氧化状态更疏水。结果,补充电子会降低链的转换温度并由此而引起折叠。
含有疏水残基(如苯丙氨酸)的生物聚合物能够在压力下把各种变化转换成运动。在低压时链折叠和较髙压力时,链伸展以促进产生五角形的水结构。我们最终能够通过吸附光敏基团把光转换成运动:当与适当波长的光碰撞时,偶氮苯或肉桂酰胺将从比较疏水的状态转换成比较亲水的状态。
由于生物化学家能够在分子水平上拆开活的细胞或将细胞的组分精确地合成复制,这就有可能确定逆温转换机制事实上是否是活的生物体所使用的一种机制。所有可利用的证据都指向这个方向。首先,对于操纵蛋白质的折叠和展开来说,它称得上是最有效的机制。按理说,自然选择应当早已发现,这种机制已经经历了30亿年。实际上,在聚合物将其化学能转换成运动来说,它称得上是最有效的方法。随带电荷的亚单位之间的排斥而伸展或收缩的聚合物几乎没有这种效应,原因是围绕的水分子屏蔽了彼此的电荷。例如,聚异丁烯酸必须将15倍于我们研究的一个生物聚合体的许多残基从有电荷转换成无电荷,才能完成同一工作。
其次,在大多数生物体中能量选择性的流动的磷酸盐——在ATP(三磷酸腺苷)形式及其等价体中——在操纵转换温度的变化方面是特别适合的。加入磷酸盐的有效性是将羧酸转换成羧酸盐的4倍。被结合的ATP,在这些用途方面作为多电荷的磷酸盐基团是等效的。
在我们研制的分子链上试验磷酸盐的效应决不是如此简单的。我们必须通过把酶加到围绕氨基酸的液体内而创建含有可以容易地被磷酸化或去磷酸化氨基酸序列的聚合物。所取得的成功来自使用了称为RGYSLG(精氨酸-甘氨酸-酪氨酸-丝氨酸-亮氨酸-甘氨酸)的亚单位和叫做蛋白激酶的酶(蛋白激酶把磷酸盐加到丝氨酸残基上)。把这种顺序的百分之三的部分插入我们的链中,我们就制造成了在蛋白激酶存在下会伸展的聚合物。能够移走磷酸酯(盐)的碱性磷酸酯酶,可使这些链再度折叠。
我们在我们所创建的生物聚合物中所证实的磷酸盐操纵机制也可以控制折叠和细胞内蛋白质的组装。例如,单个的蛋白质在体温时可以折叠成闭合的状态,这是因为对要形成围绕蛋白质的疏水表面的五角形结合水来说,蛋白质的环境是过于热了。结合到蛋白质上单一磷酸盐或ATP分子会让水去包围失去结构形态的区域,从而向开放状态的平衡方向变化。
通过强制打开这样一种蛋白质,磷酸盐可能会暴露键结合位点,否则会使其他蛋白质无法察觉,从而使重要的相互作用容易进行。例如,“热休克”蛋白质(也叫做chaperonins)有助于具有显著疏水表面的一些蛋白质正确地折叠。最重要的是,这样一种chaperonins与结合ATP肌肉的成分有一种同质的形态。
我相信,逆温转换机制是绝大多数生物的能量转换的核心。因此,把食物中的化学能转换成ATP的这种氧化磷酸化作用的过程,在很大程度上,能够根据这种机制来理解。在细胞内,辅基的氧化作用和还原作用产生质子的梯度,从而操纵磷酸化反应以形成ATP。所有这些能量转换的步骤可以由蛋白质随转换温度的变化而折叠或伸展来完成。
建造与ATP及其有关的酶类反应的生物聚合体会帮助研究人员了解许多细胞的机制。这些知识最终可以导致合成肌肉的置换物和组织的变种。生物弹性材料作为组织的替代品是特别有希望的。因为它们能够在一致性的范围内被制造出来。结果可能是凝胶状的、橡胶状的或像塑料一样的刚体的结果,这要随聚合物中的氨基酸而定。和暂时或永久地被代替的组织的弹性相一致是把合成的组织与它周围的活组织进行整合的关键。细胞能够感受到被组织接受的这种张力,伸展(或收紧)显然可推动细胞为其特定位置去适当地做功而引起的化学反应。
可是,在生物弹性聚合物成为满意的组织替代品之前很久,它们在体内就已作为其它用途的宿主。移植到兔子和大鼠体内的聚(VPGVG)的弹性薄片与大多数其它材料不同,它显然单单是被免疫系统所忽视了。直接应用这种生物相容性大多数可以阻止粘连,从而避免了手术或外伤后常常发生的痛苦的和潜在的危险的过度生长。实质上作为内部绷带的聚合物薄片能够使邻近的组织层不致融合在一起。
在Naval医学研究所工作的Lynne D. Hoban、Taffy Williams和Adam McKee把一个消过毒的聚(VPGVG)薄片放进手术过程中通常易引起粘连现象的大鼠的腹腔内。他们发现,该材料减弱了有害性组织的生长,在他们试验中的80%的实验对象都达到了统计学上的差异不显著性水平。发生粘连的有一半是由于手术期间薄片已被撕裂所造成的。在其余的场合,组织过度生长吞没了全部薄片,但聚合物实际上仍然容易与粘连分开。
这些材料在眼科手术的初步试验中看来也很有希望。外科医生用复位一些控制凝视的肌肉的方法来矫正斜视(眼睛的一种不正常排列)。遗憾的是,这种方法在肌肉上要留下伤痕组织。亚拉巴马大学Birmingham’s(伯明翰)眼科基础医院的Federick J. Elsas对兔子动手术,发现切伤的肌肉隐藏于生物聚合物覆盖中,从而防止了伤痕的出现。将这些有弹性的包扎材料用于矫正视网膜脱落的手术看来也是有希望的;这些有弹性的包扎材料能够围绕在眼球的周围压迫眼球,并使用外科手术用的激光待视网膜连接后在原位促进其愈合。
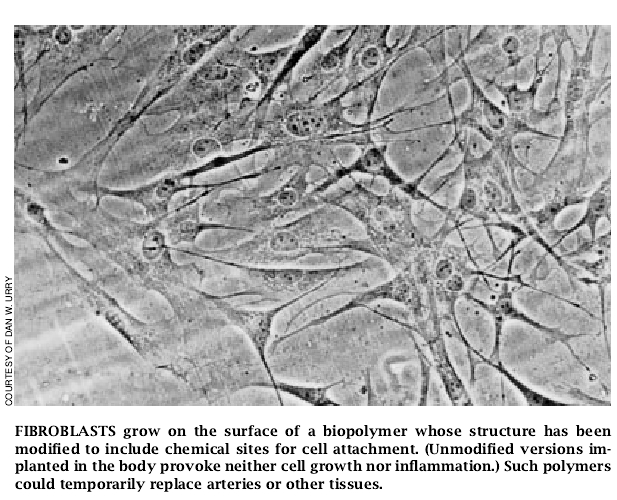
合成的聚合物链还能够加进生物学上具有活性的氨基酸顺序。对于每40个单位的GVGVP来说,含有一单位的附着于已知细胞顺序的甘氨酸-精氨酸-甘氨酸-天冬氨酸-丝氨酸-脯氨酸(GRGDSP)交联薄片仍就是清晰的与有弹性的。然而,细胞并未忽视这种材料,而是粘附它、扩散、生长到融合。例如,用于人造血管的暂时性、功能性的搭架生物材料可以被设计制造出来,以便细胞得以侵入并将此基质转变成天然的组织,即使当聚合物起着细胞所需的结构作用亦如此。
比较复杂的生物聚合物也许能够模拟的并不是组织的机械功能,而是它们的化学行为。含有治疗药剂的一种装置可以在整个过程中以固定的速率释放药物或者通过加入传感机制的方法——称为诊断-治疗对的Ralph Christoffersen核糖酶药物来释放。
这类持续释放药物的聚合物可能依赖将无电荷的碳氧酰胺(OONH2)转变成羧基(COO-)的化学装置,而此过程的历期能够从几天到数十年之久。在将诊断与治疗结合起来的装置中,设计人员可能将酶类和辅基耦合到分子的链中,以便使机体内的环境条件会自动地控制折叠和展开。例如,控制糖尿病的生物聚合物就可以把耦合的辅基加到葡萄糖还原酶上。随着血糖的增加,葡萄糖还原酶会将电子从辅基上转移到附近的葡萄糖分子中去。新的亲水的聚合物就会膨胀而释放胰岛素。
有弹性的生物聚合物同时也能以更为普通的方式使用。由于控制折叠的转换过程通常是可逆的,这些分子能够把机械的做功转换成化学的或其它形式的能量。恰如易于将光、热或压力转换成运动一样。生物分子脱盐的植物可以依赖在盐存在时通常会皱缩的聚合物带。这种带在含盐分的水中会伸展,为水分子开放空间(但不溶解盐〕,在其疏水侧链的周围形成五角形的结构。在放电槽中的卷滚会压出纯水。
此外,更现实的使用方法来自把聚合物与水的吸收作用和温度敏感性相结合:一种有独特效果的可生物降解的婴儿尿布。制造分子链尿布考虑到了尿布所经受的逆温转换正好低于皮肤的正常温度。当液体接触到内表面时,该处的分子就会将其吸收(吸湿),但这些分子仍会保持其折叠状态。聚合物在低温时链展开的习性,会自发地吸收流动的液体远离温暖的身体并流向冷却的外表面。干的基质可以吸收10倍于自重的水,而使用后这种分子链尿布就会很容易地通过环境中的微生物将其降解。基因工程的工程师们现在已经能把制成一些生物弹性材料的DNA顺序放进大肠杆菌内,在发酵罐中大量生产,最终可能使生物材料的成本与现在用在一次性使用的尿布中的有机聚合物的成本相竞争。
这种简单的聚合物产品设计可能只是弹性生物聚合物的许多非医学用途之一。生物弹性材料有如此多的潜在用途,部分原因是它们能够被设计成可相互转换如此众多的能量形式。它们对其周围环境发生的任何变化几乎都能感受到,而且它们还能产生化学的、电的或物理的反应。一旦这些生物弹性材料能以商业规模进行生产,它们应能廉价到足以在几乎任何地方使用。而且,植入的分子钟,一旦它们的工作寿命完结时,就会让由它们制造出的产品适度降解。
到下一个世纪,生物机械装置也许会像本世纪所使用的电器设备那样,进入千家万户的日常生活中,我的同事和我期盼着繁忙地设计有弹性的生物分子机构的将来的到来。
【赵裕卿/译 胡天其/校】
请 登录 发表评论