设想一下我们制造出只有细菌或分子那么大的“汽车”、“飞机”或者“潜艇”时的盛况吧:向人体注射微小的机器人医生,我们就可以对病灶进行定位甚至排除致病因素,例如清除人体动脉内积聚的斑块,或者清除可能诱发阿尔茨海默病(Alzheimer’s disease)的蛋白质沉积;我们还可以将纳米机器人“派往”桥梁钢筋或者飞机机翼等材料中,让它们修复肉眼看不见的内部裂纹,从而阻止这些微小裂纹变大引发灾难性后果。
近年来,化学家已成功研制出一系列只有分子大小的构件,可作为精密机电系统的零部件。美国莱斯大学的詹姆斯·图尔 (James Tour)及其同事,就用4个巴基球(buckyball,足球状碳分子)充当车轮,制造出了大小只有人体细胞1/5,000的“分子车”。
打开这款纳米车的“引擎盖”,你会发现它没有马达。到目前为止,图尔的纳米车还只能通过与周围其他分子的随机碰撞而运动,这个过程在物理上叫做布朗运动(Brownian motion)。换句话说,我们目前遇到的最大问题就是,已经学会制造分子机器,但还不知道如何驱动它们。
在活细胞甚至更小的尺度下,上述工作会遭遇到一些奇特的挑战。对纳米车而言,空气和水膜就像黏稠的糖浆,而沿途的布朗运动也会很容易让小车偏离精心设计的行进路线。在这样的条件下,即使我们能够把现有的汽车或电吹风里的马达缩小到纳微米尺度,这些器件也根本无法启动。
其实,大自然早已为我们提供了许多纳米马达的样本。只须看看活细胞的新陈代谢和分裂过程,我们就能了解这类马达的各种功能。活细胞利用它们完成细胞自身的形变、使分裂中的染色体分开、构建蛋白质骨架、摄取营养物质、向各处传送化学物质等等。所有这些马达,不论是驱动肌肉收缩的,还是驱动细菌鞭毛(flagella)做螺旋状运动的,它们的基本原理都是:将通常以三磷酸腺苷(Adenosine Triphosphate,ATP)形式储存的化学能转化为机械能。这些过程都需要用到催化剂,一种有利于化学反应(如ATP的降解)进行的物质。利用类似原理,近来研究人员在制备人工纳米马达方面,已取得一系列令人振奋的成果。
2004年,我们在美国宾夕法尼亚州立大学的研究小组开发出一种简易纳米马达,能够将储存于燃料分子中的能量催化转化为驱动力。哈佛大学的鲁斯捷姆·伊斯马吉洛夫(Rustem Ismagilov)和乔治·怀特塞德斯(George Whitesides)于2002年报道了他们研制的体积相对较大的催化马达。他们制作了几厘米长的船,并将具有催化作用的条状金属铂作为尾舵,把这个船放进装有水和过氧化氢(H2O2)混合液的容器中,它立即在液面上运动起来。铂加速过氧化氢分解成氧气和水,产生氧气气泡,通过反作用力推动小船前进,这与火箭升空的原理类似。我们工作的灵感正是来源于此。
缩小尺寸
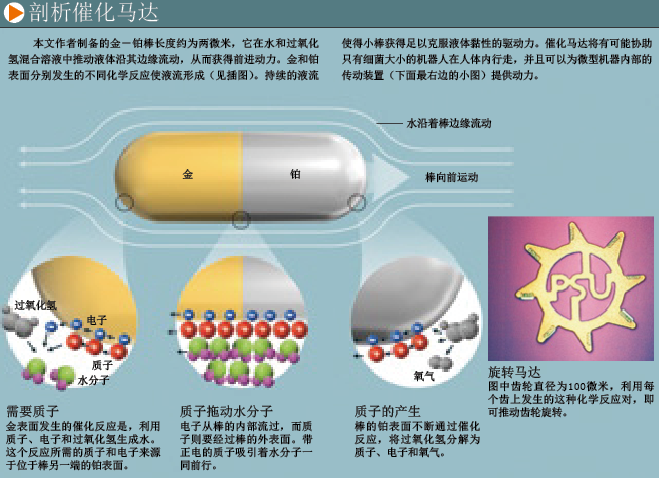
我们将哈佛大学设计的马达缩小,做出来的金-铂小棒只有一个细菌细胞(2微米)那么长,宽度只有细菌的一半(350纳米)。哈佛大学的马达漂浮在液面上,而我们的纳米催化棒则浸渍在所需的燃料液体中,与细胞中由ATP提供动力的分子马达所处的环境相似。溶液中的小棒可以立即自发地以每秒数十微米的速度运动起来,这与微观世界中的活体细菌运动方式惊人地相似。
科学研究中经常出现这种情况:根据某种假设来设计一个实验,反过来证明该假设不成立。我们此前认为纳米棒从背部喷出微小气泡,并借助反作用力(recoil)向前运动。但实际上发生的事情更有趣,因为纳米技术告诉我们,对微观尺度的运动,我们必须从独特的视角和思路来观察。
在宏观尺度上,反作用力是很容易理解的。当有人游泳或划船时,他们的手、腿或桨向后划水,反作用力就会将人体或船向前推进。在停止划水的时候,游泳者或船只还可以继续向前滑行一段,能滑行多远则取决于黏滞力(viscous force,即向后的拖曳力)和惯性(inertia,物体保持运动速度的能力)。拖曳阻力与物体的宽度成正比,惯性则与物体的质量成正比,或者说与物体宽度的三次方成正比。随着物体体积变小,惯性作用的减小速度将远远大于拖曳力,可以忽略不计,因此在这种情况下,拖曳力将成为决定性因素。对微观尺度而言,任何滑行都会在大约1微秒内结束,滑行距离不超过0.01纳米。因此,微小物体在水中的游动就像在浓稠的蜂蜜中跋涉。纳米马达无法借助任何惯性力来推动它前行,预想的惯性推进计划(如利用反冲气泡漂流)失败。
我们的纳米棒实际上是通过持续不断施加一个力来克服黏滞拖曳,而不是借助滑行的方式来运动的。在棒的铂端,单个过氧化氢分子分解得到一个氧分子、两个电子和两个质子。而在棒的金端,电子和质子通过与一个过氧化氢分子结合产生两个水分子。这种反应使得棒的一端存在多余质子,而另一端缺乏质子;因此,质子必然会沿着纳米棒表面从铂端运动到金端。
与水中所有的正离子一样,质子会吸引水分子中的负电荷区域,因此,它会拖动水分子跟着它前行,根据牛顿的作用力与反作用力定律,这将对纳米棒施加一个反方向的作用力 (参见下页框图)。
这里我要感谢我们的学生,以及美国宾夕法尼亚州立大学的其他合作者文森特·H·克里斯皮(Vincent H. Crespi)、达雷尔·韦莱古尔 (Darrell Velegol)和杰弗里·卡奇马克(Jeffrey Catchmark)的帮助。如果上述原理成立的话,其他几种纳米催化马达的设计工作即可由此展开。美国得克萨斯大学奥斯汀分校的亚当·赫勒(Adam Heller)研究组和亚利桑那州立大学的约瑟夫·王(Joseph Wang)研究组的工作证明,不同燃料的混合物(例如葡萄糖与氧混合,或者过氧化氢和肼混合)能够让纳米车跑得比在单一燃料中更快。
鉴于自由悬浮在溶液中的金属纳米棒会在其中移动,那么如果将一个金属结构固定在过氧化氢中,它就会驱使流体在固体与液体的界面上流动,这将有可能为流体中的其他物体提供驱动力。我们已经在镀了一层银膜的金表面演示过这种驱动流体的效应。
方向操控
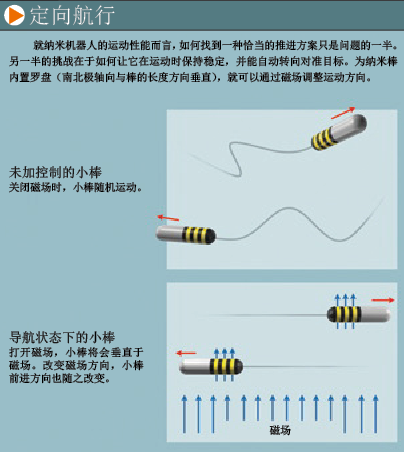
我们最初设计的液浸纳米棒马达装置的运动方向是随机的,而且会因环境中的布朗运动而不断随机转向。但在实际应用中,我们必须采取一些方法来引导它们到达目的地。
我们一开始试图利用磁场来解决这个问题(参见第42页框图)。我们在纳米棒中嵌入镍盘。对外加磁场而言,这些小盘的作用就像微型罗盘,它的南北极轴线垂直于燃料棒的长度方向。将冰箱磁贴放置到距离小棒几毫米处,磁贴施加在棒上的扭转力将使小棒摆脱因布朗运动而产生的随机转动。此时,只有沿棒长度方向的力能发挥作用,这个力由催化反应提供。这样,我们的纳米棒就将沿直线运动,并可以通过转动磁铁来改变棒的前进方向。这种方式与某些细菌利用微弱的地磁场为自己导航的行为类似。类似的马达可在微磁场中定向运动,沿着磁力线转弯或调头。
2008年,克里斯皮和本文作者阿尤斯曼·森证明,在流体环境中,这种磁导航马达可以拉动体积比它大10倍的塑料球形“货仓”。利用这种“货车”,人们可以进行许多有趣的应用研究:它们可以为人体内特定的细胞输送药物,或者将“货车”与纳米轨道上的其他分子化学键合,通过这种方式沿纳米尺度的流水线传送分子。
在某些情况下,对纳米机器人进行外部导航有一定应用价值;但在另外一些情形下,纳米机器人的自主移动则显得至关重要。最近,韦莱古尔和森惊奇地发现,催化纳米小棒能够采用类似于细菌“追踪面包屑”的化学方式前行。细菌运动时会因外部干扰而随机转向,因此它的行动过程可看成一段接一段的直线运动。一旦它直行的方向恰巧沿着化学梯度增加的方向(例如,离食物越近,气味越浓),那么细菌的直行距离将增加。由于在这个方向的直行距离大于其他方向,因此尽管细菌没有直接为自己导航的方法,但最终它们还是会在食物处汇集,这种方式叫做趋化作用(chemotaxis)。
我们的纳米马达运动速度随燃料浓度的提高而提高,这种趋势可以有效地增加直行距离。最终结果表明,所有运动总体来说都是朝着靠近燃料源(例如吸附了过氧化氢的凝胶颗粒)的方向前进的(参见第42页下方的图片)。
最近,本文两位作者还证明,可以通过光线,即利用这种马达粒子的趋光性(phototaxis)来驱动它。这些粒子使用光能将分子分解,从而得到正、负离子。两种离子以不同的扩散速度离开马达表面,从而建立起电场驱使粒子运动。分解出的离子具有不同的性质并带有不同电荷,将分别朝着和背离光强最强的区域运动。该项技术可以派生出另一个有趣的应用,即利用其中一些粒子作为“捕食者”来捕获其他“猎物”粒子。在这种情况下,一类粒子会释放出离子诱导另一类粒子向它靠近,与白血球追捕细菌的过程类似。
上述基于趋化作用和趋光性原理的纳米机器人仍处于原理验证阶段,但它们将有助于设计出自主化的“智能”纳米机器人。这些机器人将有能力主动移向目标,可能会从生物体内或周围环境中含量丰富的葡萄糖或其他燃料中获取能量。我们的工作可以作为设计这种新型机器人的一个起点,使它们能通过化学方式彼此交流,并执行群体任务,例如整体移动和排列图案。
更小的尺度
虽然这些能够进行集体行动的颗粒是“无生命”的,它们的运动所遵循的物理规律却与活细胞相似。因此,纳米马达方面的研发工作不但能从生物学中得到启发,反过来也有助于揭示生命体系中运动部件的工作原理。我们在研究催化纳米马达过程中总结出一条理论:纳米马达通常的运行速度应该与它的线性尺寸(如长度或宽度)成正比。这个比例关系的事实基础是:阻力与线性尺寸成正比;催化反应速率与物体表面积成正比。
美国宾夕法尼亚州立大学的生物学家詹姆斯·H·马登(James H. Marden)已经发现了马达质量与最大可输出力之间的一种更具普遍意义的比例关系。小到分子马达,大到喷气发动机,所有的发动机都遵循这一比例关系:马达越小,运动速度越慢。对催化纳米马达而言,它们的大小存在极限(约50~100纳米),小于这一极限,布朗运动的影响将会超过催化反应所产生的推进作用。因此,微米大小的细菌是生物界最小的自由游泳物体。小于这个尺度,流体中的物质将因为剧烈的布朗运动而无法保持稳定的前进方向。事实上,自然界中所有的分子马达,包括肌蛋白和ATP酶,要么被强制地沿着特定轨道运行,要么被嵌入膜中。未来的分子机器人都将面临同样的情况。
棘齿传送
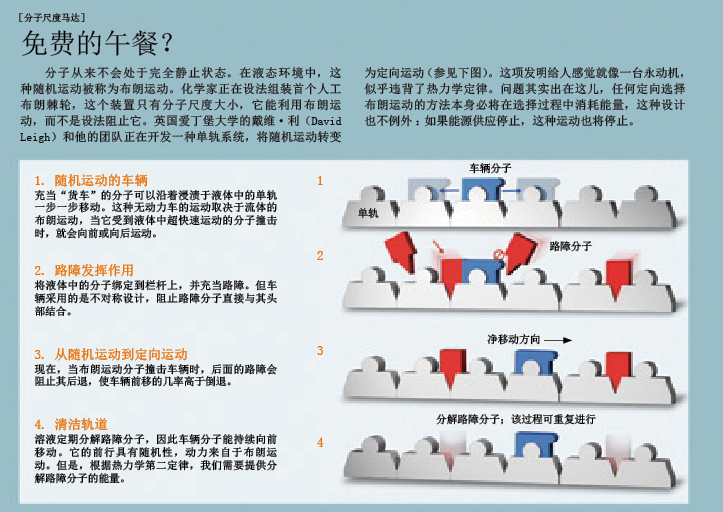
对分子尺度的马达而言,如果和我们的纳米棒一样单靠表面催化剂来提供动力,也许还不足以克服布朗运动,不管能否对它的运动进行控制。但是大自然已经找到了一种方法,可以利用布朗运动为我们工作,而不是去抑制布朗运动。许多生物马达都基于布朗棘轮(Brownian ratchet)原理,即化学催化产生的能量并不是用来产生特定方向上的运动,而是用于允许朝向目标方向的布朗运动,同时阻止反向布朗运动。近年来,研究人员已经开始尝试制备首个人工布朗棘轮(参见下页插图)。
美国北卡罗莱纳州立大学的奥林·韦列夫(Orlin Velev)和同事们采用了另外一种办法来实现推进和导航。他们最近的工作展示了在没有燃料的情况下,如何推动液体中的物体前进。研究人员在微型船上安装了一个二极管(只允许电流单向流动的装置),并施加了一个交变电场。在小船附近区域,二极管将交变电场转换成静电场。这个静电场具有恒定的方向,因此可以产生一个净推力。
由于是外部供电,催化纳米马达的比例定律在二极管马达上就不管用了。韦列夫的工作表明,厘米至毫米尺度的二极管马达的速度与外形尺寸无关,这一点与理论相符。他们的结果显示,在相当于人体细胞的尺度上(几十微米),这种马达的功率相当强劲。
随着计算机芯片技术的不断进步,现代的二极管尺寸可以远低于微米量级。利用化学合成方法,人们早已制备出长度只有2~3纳米的分子二极管。因此,制作同时具备推进、导航和传感元件的微芯片已成为可能。也许有一天,我们可以利用射频电场,对由二极管供电且不会被人体吸收的外科微型手术装置进行无线遥控。最终,这种微型手术装置可以附带一个非常细的针,通过遥控方式抵达目的地。
1959年,物理学家理查德·费曼(Richard Feynman)在一个前瞻性的讲座《在底部还有很大空间》(There's plenty of room at the bottom)中,提到了机器尺度和信息存储系统的极限问题。至少从那个时间算起,科学家(包括科幻小说作家) 已开始构想纳米机器。费曼指出,已知物理定律在分子尺度以上是有效的。因此,除了要面对制作工艺方面显而易见的技术挑战外,我们没有任何理由不去制造,甚至工业化批量生产具有原子级精度的分子部件。
在过去几十年中,费曼的演讲一直激励着纳米技术研究。同时,人们对活细胞的普遍认识已从各种各样进行代谢反应的酶,转向类似于一个由纳米马达驱动的瑞士钟表。因此,从各方面讲,细胞正是费曼设想的分子工厂。
现在,研究人员已经从生物马达上学到了不少关于如何制造非生物马达的知识,但对于该尺度下的催化行为,我们仍然知之甚少。毫无疑问,今后我们会以现在还无法想象的方式,让这些知识服务于生物医学、能源转化、化学合成及其他领域。
请 登录 发表评论